题目内容
15.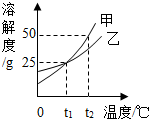 如图是甲、乙两种物质的溶解度曲线,下列说法中不正确的是( )
如图是甲、乙两种物质的溶解度曲线,下列说法中不正确的是( )| A. | t2℃时,甲的溶解度为50g | |
| B. | t2℃时,75g甲的饱和溶液中加100g水得到20%的溶液 | |
| C. | t1℃时,甲、乙两种物质的饱和溶液中溶质质量分数相等 | |
| D. | t2℃时,各100g饱和溶液降温至t1℃,析出固体甲多于乙 |
分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;t2℃时,甲的溶解度为50g正确;t2℃时,75g甲的饱和溶液中有25g甲,加100g水得到溶液的质量分数=$\frac{25g}{175g}×100%≈14.3%$,20%是错误的;t1℃时,甲、乙两种物质的饱和溶液中溶质质量分数相等正确,因为它们在该温度下有交点;t2℃时,各100g饱和溶液降温至t1℃,析出固体甲多于乙正确,因为甲的溶解度随温度的升高变化比乙大.
解答 解:A、由溶解度曲线可知:t2℃时,甲的溶解度为50g正确,正确但不符合题意,故选项错误;
B、t2℃时,75g甲的饱和溶液中有25g甲,加100g水得到溶液的质量分数=$\frac{25g}{175g}×100%≈14.3%$,20%是错误的,错误符合题意,故选项正确;
C、t1℃时,甲、乙两种物质的饱和溶液中溶质质量分数相等正确,因为它们在该温度下有交点,正确但不符合题意,故选项错误;
D、t2℃时,各100g饱和溶液降温至t1℃,析出固体甲多于乙正确,因为甲的溶解度随温度的升高变化比乙大,正确但不符合题意,故选项错误;
故选B
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
6.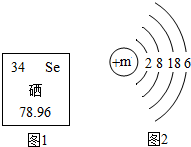 紫薯因富含硒元素被誉为“抗癌大王”.如图是硒元素在周期表中的单元格以及微粒结构示意图.下列说法不正确的是( )
紫薯因富含硒元素被誉为“抗癌大王”.如图是硒元素在周期表中的单元格以及微粒结构示意图.下列说法不正确的是( )
 紫薯因富含硒元素被誉为“抗癌大王”.如图是硒元素在周期表中的单元格以及微粒结构示意图.下列说法不正确的是( )
紫薯因富含硒元素被誉为“抗癌大王”.如图是硒元素在周期表中的单元格以及微粒结构示意图.下列说法不正确的是( )| A. | 硒化钠的化学式为Na2Se | B. | 硒的原子核内中子数约为45 | ||
| C. | 图2中m的值为36 | D. | 硒位于元素周期表中的第四周期 |
3.下列符号中,锰元素是+6价的是( )
| A. | Mn02 | B. | MnSO4 | C. | MnO4- | D. | Mn042- |
10.为相对原子质量的测定作出卓越贡献,主持测定了铟、铱等相对原子质量新值的科学家是( )
| A. |  侯德榜 | B. |  拉瓦锡 | C. |  门捷列夫 | D. |  张青莲 |
7.下列图象中有关量的变化趋势与对应叙述关系正确的是( )
| A. | 分别向盛有等质量铝粉和镁粉的两个烧杯中,不断滴加等浓度的稀硫酸.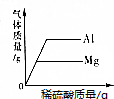 | |
| B. | 在密闭容器中点燃一定量的氢气和氧气的混合气体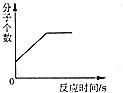 | |
| C. | 向硝酸银、硝酸铜混合溶液中加入一定量的锌粉,充分反应后过滤,得到无色液体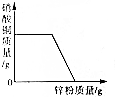 | |
| D. | 向一定量的稀盐酸中不断加入石灰石粉末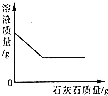 |
4.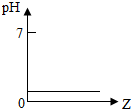 向稀盐酸中加入Z物质,其pH变化情况如图所示,则Z物质是( )
向稀盐酸中加入Z物质,其pH变化情况如图所示,则Z物质是( )
 向稀盐酸中加入Z物质,其pH变化情况如图所示,则Z物质是( )
向稀盐酸中加入Z物质,其pH变化情况如图所示,则Z物质是( )| A. | H2O | B. | AgNO3固体 | C. | 浓盐酸 | D. | KOH固体 |