题目内容
现要配制50g质量分数为12%的氯化钠溶液,需要氯化钠 g,水 mL,配制过程中应选用 的量筒.(量筒的规格有:10mL、50mL、100mL、200mL)
考点:一定溶质质量分数的溶液的配制,有关溶质质量分数的简单计算
专题:溶液、浊液与溶解度
分析:利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.从减小实验误差的角度去选择量筒的量程,据此进行分析解答.
解答:解:溶质质量=溶液质量×溶质的质量分数,配制50g质量分数为12%的氯化钠溶液,需氯化钠的质量=50g×12%=6g;溶剂质量=溶液质量-溶质质量,则所需水的质量=50g-6g=44g;水的密度为1g/mL,则根据V=
=
=44mL.
选取量筒时,尽量选用能一次量取的最小规格的量筒,则量取44mL水,应用50mL量筒.
故答案为:6;44;50mL.
| m |
| V |
| 44g |
| 1g/mL |
选取量筒时,尽量选用能一次量取的最小规格的量筒,则量取44mL水,应用50mL量筒.
故答案为:6;44;50mL.
点评:本题难度不是很大,掌握溶质质量分数一定的溶液的有关计算、量筒的使用方法等是正确解答本题的关键.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
 在一烧杯中盛有24.3g Na2SO4和NaCl组成的固体混合物,加入100g水使Na2SO4和NaCl全部溶解.向其中逐渐滴加溶质质分数为20%的氯化钡溶液.生成沉淀的总质量与所滴入氯化钡溶液的质量关系曲线如图所示,请根据题意回答问题:
在一烧杯中盛有24.3g Na2SO4和NaCl组成的固体混合物,加入100g水使Na2SO4和NaCl全部溶解.向其中逐渐滴加溶质质分数为20%的氯化钡溶液.生成沉淀的总质量与所滴入氯化钡溶液的质量关系曲线如图所示,请根据题意回答问题: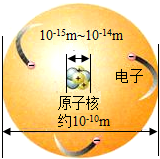 如图是锂原子的构成示意图,根据图示信息回答下列问题:
如图是锂原子的构成示意图,根据图示信息回答下列问题: