题目内容
8.小明为了测定某石灰石中碳酸钙的质量分数,他取含石灰石样品25克放入烧杯中.向其中加入100克稀盐酸,二者恰好完全反应.反应结束后,称量烧杯中剩余物质的总质量为116.2克.(不包括烧杯的质量,且气体的溶解忽略不计,杂质不和盐酸反应).请计算:(1)反应生成二氧化碳的质量.
(2)石灰石中碳酸钙的质量分数.
分析 (1)利用质量守恒定律,可由反应前后质量差求出放出二氧化碳的质量;
(2)根据反应的化学方程式,计算参加反应碳酸钙质量,从而求得石灰石中CaCO3的质量分数.
解答 解:(1)生成二氧化碳的质量为:25g+100g-116.2g=8.8g;
(2)设参加反应的碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 8.8g
$\frac{100}{x}=\frac{44}{8.8g}$
x=20g
石灰石中CaCO3的质量分数=$\frac{20g}{25g}$×100%=80%;
答:(1)生成二氧化碳的质量为8.8g;
(2)石灰石中CaCO3的质量分数为80%.
点评 根据质量守恒定律分析得反应放出二氧化碳的质量,此为解答本题的计算基础,体现出对问题的分析能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.“2H”表示的意义是( )
| A. | 表示两种氢元素 | |
| B. | 表示两个氢元素 | |
| C. | 表示两个氢原子 | |
| D. | 既表示两个氢元素,又表示两个氢原子 |
20.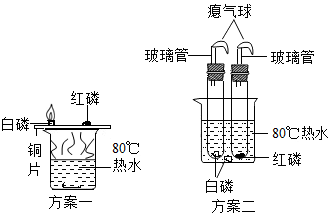 某化学小组想研究燃烧的条件,设计了如图二个实验方案,下列关于方案设计说法不合理的是( )
某化学小组想研究燃烧的条件,设计了如图二个实验方案,下列关于方案设计说法不合理的是( )
 某化学小组想研究燃烧的条件,设计了如图二个实验方案,下列关于方案设计说法不合理的是( )
某化学小组想研究燃烧的条件,设计了如图二个实验方案,下列关于方案设计说法不合理的是( )| A. | 方案一想通过铜片上白磷和红磷的现象对比,说明可燃物燃烧必须达到一定温度 | |
| B. | 方案二想通过试管中白磷和水中白磷的现象对比,说明可燃物燃烧必须达到一定温度 | |
| C. | 方案二比方案一的设计更环保 | |
| D. | 方案二的两个试管应装有氧气或空气 |
6.根据要求回答问题.
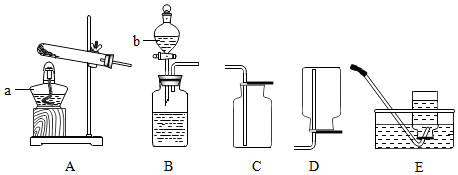
①写出仪器名称:a酒精灯; b分液漏斗;
②用氯酸钾和二氧化锰的混合物制取氧气选择的一套装置是AC或者AE(填字母);其中二氧化锰的作用是催化剂,检验收集的氧气是干燥的方法:加入硫酸铜固体,现象为白色粉末不变蓝,则是干燥的;
③实验中,有很多操作步骤必须严格按要求进行,否则或实验失败或发生危险.
④要制取0.03mol氧气,理论上至少需要氯酸钾的物质的量0.02mol;(根据化学方程式列式计算,写出计算过程)
⑤同学用制备的一瓶氧气来做铁丝在氧气中的燃烧,将一根铁丝以螺旋状绑在火柴上,点燃火柴后将铁丝慢慢伸入一瓶氧气中,将会看到剧烈燃烧,火星四射,生成黑色固体,放出大量热.但是实际上铁丝只红热一下,没其他现象,请分析铁丝没有燃烧的可能原因没有等到气泡均匀连续就收集或者铁丝表面有锈等(一条即可);
⑥实验室对氯酸钾和二氧化锰混合制氧气后剩余的固体进行了处理:(每步均充分)
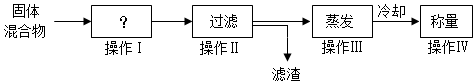
甲、操作Ⅰ的名称及最后称量的固体分析正确的是C
A.称量、二氧化锰 B.溶解、二氧化锰 C.溶解、氯化钾
乙、操作Ⅰ、Ⅱ、III中都用到的玻璃仪器名称是玻璃棒操作Ⅱ中它的作用是引流.

①写出仪器名称:a酒精灯; b分液漏斗;
②用氯酸钾和二氧化锰的混合物制取氧气选择的一套装置是AC或者AE(填字母);其中二氧化锰的作用是催化剂,检验收集的氧气是干燥的方法:加入硫酸铜固体,现象为白色粉末不变蓝,则是干燥的;
③实验中,有很多操作步骤必须严格按要求进行,否则或实验失败或发生危险.
| 必须遵循操作先后的实验 | 先进行的操作 | 后进行的操作 |
| a制取氧气 | 检查装置气密性 | 再向容器中装药品 |
| b氯酸钾制取氧气用排水发收集氧气结束时 | 先将导管从水槽移开 | 熄灭酒精灯 |
| 给药品加热 | 先均匀受热 | 再集中加热 |
⑤同学用制备的一瓶氧气来做铁丝在氧气中的燃烧,将一根铁丝以螺旋状绑在火柴上,点燃火柴后将铁丝慢慢伸入一瓶氧气中,将会看到剧烈燃烧,火星四射,生成黑色固体,放出大量热.但是实际上铁丝只红热一下,没其他现象,请分析铁丝没有燃烧的可能原因没有等到气泡均匀连续就收集或者铁丝表面有锈等(一条即可);
⑥实验室对氯酸钾和二氧化锰混合制氧气后剩余的固体进行了处理:(每步均充分)

甲、操作Ⅰ的名称及最后称量的固体分析正确的是C
A.称量、二氧化锰 B.溶解、二氧化锰 C.溶解、氯化钾
乙、操作Ⅰ、Ⅱ、III中都用到的玻璃仪器名称是玻璃棒操作Ⅱ中它的作用是引流.
 根据木炭、细铁丝在氧气中燃烧的实验图片回忆,按要求回答问题.
根据木炭、细铁丝在氧气中燃烧的实验图片回忆,按要求回答问题. 化学与生活息息相关.
化学与生活息息相关.