题目内容
通过本单元的学习,试回答下列问题
(1)金属具有很多的共同的 .例如,常温下它们都是 (汞除外),有金属光泽,大多数能导 和 ,有延展性,密度 ,熔点 .
(2)铁的化学性质比较活泼,在纯氧中燃烧的现象是 ,化学方程式为 .
(3)距今两千多年前,我国古代劳动人民已掌握了炼铁的技术,他们将炭不完全燃烧产生一氧化碳,在高温条件下利用一氧化碳将铁矿石中氧化铁还原为铁.请写出上述两个反应的化学方程式是:①
② .
(1)金属具有很多的共同的
(2)铁的化学性质比较活泼,在纯氧中燃烧的现象是
(3)距今两千多年前,我国古代劳动人民已掌握了炼铁的技术,他们将炭不完全燃烧产生一氧化碳,在高温条件下利用一氧化碳将铁矿石中氧化铁还原为铁.请写出上述两个反应的化学方程式是:①
②
考点:金属的物理性质及用途,金属的化学性质,铁的冶炼,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据已有的金属的性质、铁燃烧的现象和一氧化碳还原氧化铁的知识进行分析解答.
解答:解:(1)金属具有很多的共同的物理性质.例如,常温下它们都是固体 (汞除外),有金属光泽,大多数能导导电和导热,有延展性,密度较大,熔点较高,故填:物理性质,固体,导电,导热,较大,较高.
(2)铁的化学性质比较活泼,在纯氧中燃烧的现象是剧烈燃烧、火星四射、放出大量的热,生成黑色的固体四氧化三铁,故填:剧烈燃烧、火星四射、放出大量的热,生成黑色的固体; 3Fe+2O2
Fe3O4.
(3)①碳不完全燃烧生成一氧化碳,故填:2C+O2
2CO
②氧化铁和一氧化碳在高温下反应生成铁和二氧化碳,故填:Fe2O3+3CO
2Fe+3CO2.
(2)铁的化学性质比较活泼,在纯氧中燃烧的现象是剧烈燃烧、火星四射、放出大量的热,生成黑色的固体四氧化三铁,故填:剧烈燃烧、火星四射、放出大量的热,生成黑色的固体; 3Fe+2O2
| ||
(3)①碳不完全燃烧生成一氧化碳,故填:2C+O2
| ||
②氧化铁和一氧化碳在高温下反应生成铁和二氧化碳,故填:Fe2O3+3CO
| ||
点评:掌握常见金属的性质以及有关实验的现象是解答本题的关键,书写反应的化学方程式要注意配平.

练习册系列答案
相关题目
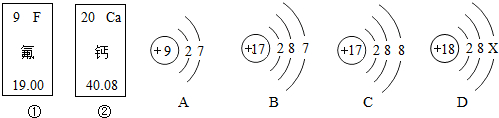
 做完“铁在氧气里燃烧”实验后,某兴趣小组有一些疑惑不解的问题,于是他们进行了以下探究活动,请你一同参与.
做完“铁在氧气里燃烧”实验后,某兴趣小组有一些疑惑不解的问题,于是他们进行了以下探究活动,请你一同参与.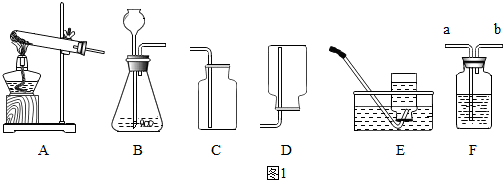
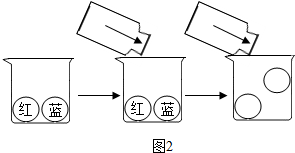
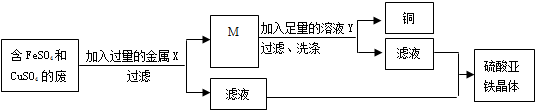
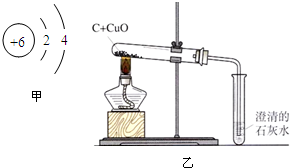 碳与碳的化合物在工农业生产及日常生活中有广泛的用途.
碳与碳的化合物在工农业生产及日常生活中有广泛的用途.