题目内容
5.现有3g碳放入盛有9g氧气的密闭容器中充分燃烧,生成二氧化碳质量为11g;现有质量为ag的蜡烛燃烧一段时间后剩余质量为bg,生成二氧化碳和水的质量分别为cg和dg,则参加反应的蜡烛质量为(a-b)g,参加反应的氧气质量为(c+d+b-a)g.分析 根据质量守恒定律可知,参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和.那么,生成物的质量总和与反应掉的蜡烛的质量之间的差即为参加反应的氧气的质量进行分析.
解答 解:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,
12 32 44
碳、氧气反应的质量比是3:8,所以3g碳放入盛有9g氧气的密闭容器中充分燃烧,生成二氧化碳质量为11g,蜡烛燃烧的反应表达式为:石蜡+氧气$\stackrel{点燃}{→}$二氧化碳+水,故有蜡烛参加反应的质量为(a-b)g;生成的二氧化碳和水蒸气的质量共是(c+d)g;据质量守恒定律可知,参加反应的氧气的质量为:(c+d)-(a-b)g.
故答案为:11,(a-b)g,(c+d+b-a)g.
点评 熟练掌握质量守恒定律的内容,知道所有的化学反应都遵循质量守恒定律,即:参加反应的物质的质量等于反应后生成的物质的质量.

练习册系列答案
相关题目
4.物质的用途与性质密切相关,下列说法错误的是( )
| A. | 铁用于制作铁锅,是由于铁有良好的导热性 | |
| B. | 金刚石可用于制作玻璃刀,是由于金刚石的硬度大 | |
| C. | 稀有气体可用作保护气,因为稀有气体的化学性质不活泼 | |
| D. | 氢氧化钠固体可用作某些气体的干燥剂,是由于氢氧化钠固体能与水反应 |
16.下列变化中,没有新物质生成的是( )
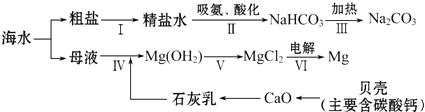
| A. | 冶炼金属 | B. | 海水制碱 | C. | 海水晒盐 | D. | 海水提炼金属镁 |
13.下列除去杂质的方法中,正确的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | ZnCl2溶液 | CuCl2 | 过量锌粉,过滤 |
| B | CaCl2溶液 | 盐酸 | 加适量 NaOH |
| C | CuO | Cu | 加水,过滤 |
| D | O2 | H2 | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
20.50克木炭和氧化铜的混合物在高温下反应后,剩余固体的质量为39克,(假设没有一氧化碳产生),原混合物中碳与氧化铜的质量比可能为( )
| A. | 1:2 | B. | 1:4 | C. | 3:20 | D. | 3:40 |
10.下列实验操作中,不正确的是( )
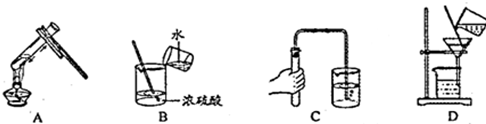

| A. | A | B. | B | C. | C | D. | D |
15.“民以食为天”.下列过程主要属于化学变化的是( )
| A. | 酿酒 | B. | 淘米 | C. | 洗菜 | D. | 碾米 |