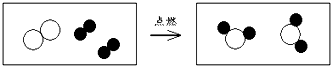
题目内容
14.海洋中蕴含丰富的资源.(1)海水淡化是解决淡水资源不足的重要方法.下列方法中,可以使海水变为淡水的是D(填字母序号).
A.滤纸过滤 B.吸附 C.沉降 D.蒸馏
(2)从海水中提炼出来的重水(D2O)可作原子能反应堆的中子减速剂和传热介质.重水中重氢原子(D)的相对原子质量是2,则重水中氧元素的质量分数为80%.
(3)从海水中制备纯碱和金属镁的流程如图所示:
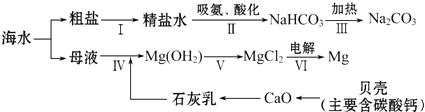
回答下列问题:
①步骤Ⅴ中所加试剂是稀盐酸.
②粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下列物质,利用过滤等操作进行除杂,则加入下列三种物质的先后顺序为cba(填字母序号).
a.适量的盐酸
b.稍过量的Na2CO3溶液
c.稍过量的Ba(OH)2溶液
③第Ⅲ步反应的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
④在海边用贝壳作原料制生石灰,比用石灰石作原料好,其优点是减少贝壳污染(写一条).
分析 (1)根据水的净化方法的原理分析解答;
(2)根据元素质量分数计算公式计算;
(3)①根据氢氧化镁与盐酸反应生成氯化镁和水进行分析;
②根据除杂质的注意事项:加入的试剂只能与杂质反应,不能与需要的物质反应,不能引入新的杂质;
③根据碳酸氢钠在加热的条件下生成碳酸钠、水和二氧化碳进行分析;
④根据污染、经济价值方面解释.
解答 解:(1)A、过滤是除去不溶性杂质的方法,不能除去水中的可溶性物质,故A错误;
B、吸附是除去水中色素、异味等不溶性杂质的一种方法,不能除去水中的氯化钠、氯化镁等可溶性盐,故B错误;
C、沉降是使大颗粒不容物快速沉淀下来,不能除去水中的可溶性物质,故C错误;
D、蒸馏是通过加热的方法将水变成水蒸气,再冷凝成水的方法,可以得到最纯的蒸馏水,故可将水淡化,故D正确;
故选:D;
(2)重水中的重氢原子的相对原子质量为2,则氧元素质量分数为:$\frac{16×1}{2×2+16×1}$×100%=80%;
(3)①氢氧化镁为白色沉淀,与盐酸反应生成氯化镁;
②粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,所加试剂的顺序是加稍过量的Ba(OH)2溶液,除去MgSO4,再加稍过量的Na2CO3溶液,除去CaCl2,最后加适量的盐酸,中和前后过量的Ba(OH)2和Na2CO3;
③第Ⅲ歩反应是碳酸氢钠在加热的条件下生成碳酸钠、水和二氧化碳,化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
④在海边用贝壳作原料制生石灰,比用石灰石作原料的优点既可减少贝壳污染又可提高经济效益.
故答案为:(1)D;
(2)80%;
(3)①稀盐酸(或HCl);
②cba;
③2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
④减少贝壳污染(或提高经济效益、减少资源浪费等).
点评 本题考查较综合,涉及内容较多,为常见题型,利用所学知识结合流程图信息是解答本题的关键,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 空气中各成分按体积分数计算,大约含有78%的氮气、21%的氧气、0.94%的稀有气体、0.03%的CO2以及0.03%的其他气体和杂质 | |
| B. | 氮气是一种化学性质比较活泼的气体 | |
| C. | 洁净的空气是纯净物 | |
| D. | 植物的光合作用是空气中二氧化碳的主要来源 |
| A. | NaClO2中氯元素的化合价为+3价 | |
| B. | NaClO2是由NaCl和O2构成的 | |
| C. | NaClO2中钠元素质量分数约为25.4% | |
| D. | NaClO2中钠、氯、氧原子个数比为1:1:2 |
【知识回放】填写对应金属的元素符号.
金属活动性顺序:K Ca Na Mg Al ZnFe Sn Pb(H)CuHg Ag Pt Au,请你在横线上
【作出猜想】猜想1:Cr>Fe>Cu; 猜想2:Fe>Cu>Cr; 猜想3:你的猜想是Fe>Cr>Cu.
【查阅资料】(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验操作 | 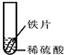 | 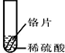 | 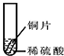 |
| 实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | 无明显现象发生(或无气泡生成,溶液也不变色) |
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应
【知识运用】将铬片投入FeSO4溶液中,反应能(填“能”或“不能“)进行,若能进行,
请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
| A. | 3O2Fe | B. | Fe2O3 | C. | Fe2O3 | D. | O3Fe2 |
| A. | 还原 | B. | 吸附 | C. | 导电 | D. | 消毒 |
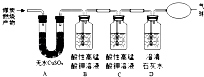 我国是世界上最大的煤炭生产国和消费国,也是世界上少数几个以煤炭为主要能源的国家之一.化学兴趣小组的同学对煤炭燃烧的主要产物产生了兴趣,请你参与:
我国是世界上最大的煤炭生产国和消费国,也是世界上少数几个以煤炭为主要能源的国家之一.化学兴趣小组的同学对煤炭燃烧的主要产物产生了兴趣,请你参与: