题目内容
20. 如图是A、B、C三种物质的溶解度曲线,请回答:
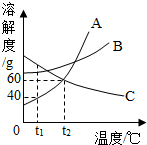
如图是A、B、C三种物质的溶解度曲线,请回答:(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A;
(2)当A中混有少量B时,可用降温结晶方法提纯A;
(3)t2℃时,40gA物质加入到50g水中不断搅拌形成溶液质量是80g.
分析 根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
从溶液中结晶的方法有两种:蒸发结晶和降温结晶,物质的溶解度受温度变化影响较小时,应该用蒸发结晶;物质的溶解度受温度变化影响较大时,应该用降温结晶;
根据物质的溶解度曲线、溶质质量、溶剂质量可以判断配制的溶液质量.
解答 解:(1)由溶解度曲线可知,t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A;
(2)由溶解度曲线可知,A的溶解度受温度变化影响较大,B的溶解度受温度变化影响较小,当A中混有少量B时,可用降温结晶方法提纯A;
(3)由溶解度曲线可知,t2℃时,A的溶解度是60g,40gA物质加入到50g水中不断搅拌,只有30gA完全溶解,形成溶液质量是80g.
故填:C>B>A;降温结晶;80.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
相关题目
11.甲、乙两种固体物质的溶解曲线如图t2℃时,分别盛甲、乙两种物质饱和溶液的试管放在装有同温度水的烧杯中,如图2.不考虑溶剂的蒸发.根据图象和有关信息判断,下列说法中错误的是( )
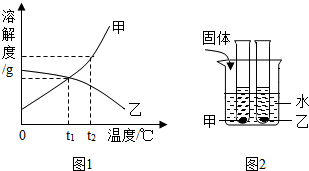

| A. | t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为:甲>乙 | |
| B. | 将甲、乙两种物质的饱和溶液都从t2℃降至t1℃时,两种溶液中溶质的质量分数相等 | |
| C. | 向烧杯的水中加NH4NO3固体后,只有盛放甲溶液的试管中有晶体析出 | |
| D. | 向烧杯的水中加NaOH固体后,只有乙溶液中溶质的质量分数变小 |
8.液氧转化为氧气的过程中,发生变化的是( )
| A. | 元素种类 | B. | 分子间的间隔 | C. | 分子的种类 | D. | 分子的总数 |
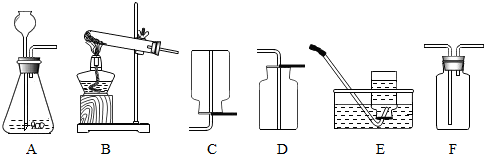
12.对如图实验的分析说明不正确的是( )


| A. | 该实验说明一氧化碳具有还原性 | |
| B. | 该实验说明生成物二氧化碳的密度比空气大 | |
| C. | 该实验说明一氧化碳和氧化铜的反应需要加热 | |
| D. | 该实验可以防止有毒的一氧化碳气体对空气的污染,同时又可以充分利用能源 |
9. 常温下,在两个各盛有100mL水的烧杯中,分别加入相同质量的甲、乙两种物质,使其充分溶解,并恢复到原温度,结果如图所示.下列说法中正确的是( )
常温下,在两个各盛有100mL水的烧杯中,分别加入相同质量的甲、乙两种物质,使其充分溶解,并恢复到原温度,结果如图所示.下列说法中正确的是( )
 常温下,在两个各盛有100mL水的烧杯中,分别加入相同质量的甲、乙两种物质,使其充分溶解,并恢复到原温度,结果如图所示.下列说法中正确的是( )
常温下,在两个各盛有100mL水的烧杯中,分别加入相同质量的甲、乙两种物质,使其充分溶解,并恢复到原温度,结果如图所示.下列说法中正确的是( )| A. | 该温度下的溶解度:甲>乙 | B. | 升高温度,剩余的甲固体继续溶解 | ||
| C. | 甲溶液可能是饱和溶液 | D. | 乙溶液可能是饱和溶液 |
10.下列关于实验现象的描述正确的是( )
| A. | 木炭在氧气中燃烧,产生红色火焰 | |
| B. | 用小木棍藮取少量浓硫酸,小木棍会逐渐变黑 | |
| C. | 浓盐酸敞口放置在空气中,瓶口会形成白烟 | |
| D. | 将蘸有紫色石蕊的干燥纸花放入盛有二氧化碳的集气瓶中,纸花变红 |
 酸、碱、盐的化学性质是初中化学的核心知识.如图A-E是初中化学常见的酸、碱、盐,其中A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为不溶于硝酸白色沉淀.:“→”表示一种物质能转化为另一种物质(部分反应物、生成物及反应条件已省略).
酸、碱、盐的化学性质是初中化学的核心知识.如图A-E是初中化学常见的酸、碱、盐,其中A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为不溶于硝酸白色沉淀.:“→”表示一种物质能转化为另一种物质(部分反应物、生成物及反应条件已省略).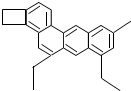 化学家TimRichard将分子结构简式像小狗的某有机物(如图所示),取名为“小狗烯”(化学式为C26H26),请计算:
化学家TimRichard将分子结构简式像小狗的某有机物(如图所示),取名为“小狗烯”(化学式为C26H26),请计算: