题目内容
18.矿泉水一般是由岩石风化后矿泉水一般是由岩石风化后被地下水溶解其中可溶解部分生成的,此处所指的风化是指矿物与水及二氧化碳同时作用的过程.例如,长石(KAlSi3O8)风化生成高岭土[Al2(Si2O5)(OH)4],此反应的离子方程式为:2KAlSi3O8+2H2CO3+5H2O=2KHCO3+4H2SiO3+Al2(Si2O5)(OH)4(1)可以用氧化物的形式表示硅酸盐的组成,如Na2SiO3可以写成(Na2O•SiO2),镁橄榄石(Mg2SiO4)可以表示为2MgO•SiO2. 将上述复杂硅酸盐改写成氧化物形式:
①KAlSi3O8K2O•Al2O3•6SiO2;
②Al2(Si2O5)(OH)4Al2O3•2SiO2•2H2O.
(2)上述反应能够发生的原因是碳酸酸性比硅酸强,由强酸可制得弱酸.
分析 (1)根据化学式改写成相应的氧化物的形式,按照活泼金属氧化物•较活泼金属氧化物•SiO2•H2O的顺序来书写,并要遵守原子守恒来分析解答.
(2)化学反应多数遵循强酸制备弱酸的原则.
解答 解:(1)①钾的氧化物为K2O,铝的氧化物为Al2O3,硅的氧化物为SiO2,则根据活泼金属氧化物•较活泼金属氧化物•SiO2•H2O的顺序可知,KAlSi3O8可改写为
K2O•Al2O3•6SiO2;故填:K2O•Al2O3•6SiO2;
②铝的氧化物为Al2O3,硅的氧化物为SiO2,氢的氧化物为H2O,则根据活泼金属氧化物•较活泼金属氧化物•SiO2•H2O的顺序可知,[Al2Si2O5(OH)4]可改成Al2O3•2SiO2•2H2O,故答案为:Al2O3•2SiO2•2H2O;
(2)碳酸可生成原硅酸,说明碳酸的酸性比原硅酸的强,故此反应发生的原因是碳酸酸性比硅酸强,由强酸可制得弱酸,故答案为:碳酸酸性比硅酸强,由强酸可制得弱酸.
点评 本题考查含硅矿物及材料的应用,注重将复杂化合物写出氧化物的形式的考查,注意要知道非金属元素氧化物的化学式的书写和先后顺序,还有遵循原子守恒定律,难度不大.

练习册系列答案
相关题目
8.图甲中A是一种常见的酸,它能与黑色固体B反应,B质量为8克,将NaOH溶液渐渐加入到C中,生成蓝色沉淀E和无色溶液D,蓝色沉淀E的质量与加入NaOH溶液的质量关系如图乙所示,在D中加入Ba(NO3)2溶液能生成一种不溶于稀硝酸的白色沉淀.
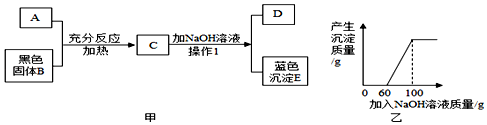
(1)A溶液中溶质的化学式为H2SO4;
(2)操作1的名称是过滤;
(3)C溶液中的含义的阳离子是H+、Cu2+,
(4)D溶液中含有什么物质呢?
小明说:只有硫酸钠;小童说:含有硫酸铜和硫酸钠;你的猜想是氢氧化钠和硫酸钠.
大家一致认为小童的说法是错误的,其理由是硫酸铜溶液是蓝色的.
(5)C溶液中硫酸铜溶质的质量.(写出计算过程)

(1)A溶液中溶质的化学式为H2SO4;
(2)操作1的名称是过滤;
(3)C溶液中的含义的阳离子是H+、Cu2+,
(4)D溶液中含有什么物质呢?
小明说:只有硫酸钠;小童说:含有硫酸铜和硫酸钠;你的猜想是氢氧化钠和硫酸钠.
大家一致认为小童的说法是错误的,其理由是硫酸铜溶液是蓝色的.
| 实验步骤 | 实验现象 | 结论 |
| 取少量无色滤液,向其中加入酚酞试液. | 溶液变红. | 你的猜想成立. |
6.下列说法中,不正确的是( )
| A. | 原子、分子和离子都是构成物质的微粒 | |
| B. | 分子和原子都是不断运动的 | |
| C. | 原子都是由原子核和核外电子构成的 | |
| D. | 任何原子核都是由质子和中子构成的 |
13.一个N2O3分子的质量为a千克,一个N2O5分子的质量为 b千克;若以氧原子质量的$\frac{1}{16}$作为标准,则NO2的相对分子质量为( )
| A. | $\frac{8(b+a)}{b-a}$ | B. | $\frac{16(b+a)}{b-a}$ | C. | $\frac{8(a-b)}{a+b}$ | D. | $\frac{a+b}{4}$ |
3.米煮熟成饭的过程主要发生的变化属( )
| A. | 机械变化 | B. | 物理变化 | C. | 化学变化 | D. | 无法确定 |
10.生活中许多变化都能产生热量,下列放热现象主要由物理变化引起的是( )
| A. | 木炭燃烧放热 | B. | 生石灰与水混合生成熟石灰放热 | ||
| C. | 白炽灯泡通电发热 | D. | 苹果腐烂发热 |
7.现有一种固体粉末状样品,已知该样品由氧化铜和铁组成.某化学小组进行了如图所示实验操作.
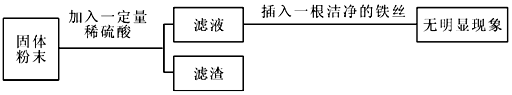
关于该实验,下列说法中正确的是( )

关于该实验,下列说法中正确的是( )
| A. | 向样品中加入稀硫酸后,一定有气体生成,且液体颜色不变 | |
| B. | 滤液中含有硫酸铜和硫酸亚铁 | |
| C. | 滤液中溶质只有硫酸亚铁 | |
| D. | 滤渣中一定有铜,不一定有铁 |