题目内容
3.下列各组离子能在pH=1的水溶液中大量共存且形成无色溶液的是( )| A. | Ag+、Cl-、Fe2+、NO3- | B. | CO32-、K+、Na+、Cl- | ||
| C. | Cu2+、OH-、SO42-、Ba2+ | D. | NH4+、NO3-、Na+、Cl- |
分析 pH为1的水溶液显酸性,水溶液中含有大量的H+.根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能大量共存;本题还要注意溶液呈无色,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:pH为1的水溶液显酸性,水溶液中含有大量的H+.
A、Ag+、Cl-在溶液中能结合生成不溶于酸的氯化银沉淀,不能在酸性溶液中大量共存,且Fe2+的水溶液显浅绿色,故选项错误.
B、CO32-、H+能结合生成水和二氧化碳,不能在酸性溶液中大量共存,故选项错误.
C、OH-、H+能结合生成水,SO42-、Ba2+在溶液中能结合生成不溶于酸的硫酸钡沉淀,不能在酸性溶液中大量共存,
D、四种离子间不能结合成沉淀、气体或水,能在酸性溶液中大量共存,且不存在有色离子,故选项正确.
故选:D.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水;还要注意是在酸性溶液中共存及特定离子的颜色.

练习册系列答案
 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
13.用“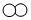 ”和“
”和“ ”代表两种不同的物质分子,它们在一定条件下能发生化学反应,反应前后的微观模型如下图所示,下列说法正确的是( )
”代表两种不同的物质分子,它们在一定条件下能发生化学反应,反应前后的微观模型如下图所示,下列说法正确的是( )
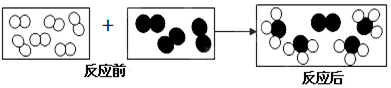
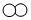 ”和“
”和“ ”代表两种不同的物质分子,它们在一定条件下能发生化学反应,反应前后的微观模型如下图所示,下列说法正确的是( )
”代表两种不同的物质分子,它们在一定条件下能发生化学反应,反应前后的微观模型如下图所示,下列说法正确的是( )
| A. | 参加反应的“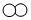 ”和“ ”和“ ”分子的个数比是2:1 ”分子的个数比是2:1 | |
| B. | 该反应有2种生成物 | |
| C. | 该反应是化合反应 | |
| D. | 每个生成物分子由3个原子构成 |
14.铁是人体必需的微量元素,菠菜因富含铁元素(化合态)而成为补铁的食物之一.小明设计实验探究菠菜中含有Fe2+ 还是Fe3+?
首先,他查阅了相关资料,得到以下信息:
①少量含Fe3+的溶液中加入硫氰化钾(KSCN)溶液,溶液变为血红色;
②在少量含Fe2+的溶液中加入酸性高锰酸钾溶液,酸性高锰酸钾溶液紫色褪去;
③稀硝酸具有强氧化性.
来源:然后,小明设计并动手做实验,实验步骤如下:
步骤一:

步骤二:分别取2mL溶液B于三支试管中,实验操作和现象如表所示:
请回答下列问题:
(1)实验步骤中的操作②和③的名称是过滤.
(2)此实验证明菠菜中含有Fe2+.
(3)请猜测一下在丙中加入稀硝酸的作用是把亚铁离子氧化成铁离子.
首先,他查阅了相关资料,得到以下信息:
①少量含Fe3+的溶液中加入硫氰化钾(KSCN)溶液,溶液变为血红色;
②在少量含Fe2+的溶液中加入酸性高锰酸钾溶液,酸性高锰酸钾溶液紫色褪去;
③稀硝酸具有强氧化性.
来源:然后,小明设计并动手做实验,实验步骤如下:
步骤一:

步骤二:分别取2mL溶液B于三支试管中,实验操作和现象如表所示:
| 试管 | 加入适量检验药品 | 实验现象 |
| 甲 | 酸性高锰酸钾溶液 | 酸性高锰酸钾溶液紫色褪去 |
| 乙 | 硫氰化钾溶液 | 溶液不变血红色 |
| 丙 | 先加入稀硝酸,再加入硫氰化钾溶液 | 溶液变血红色 |
(1)实验步骤中的操作②和③的名称是过滤.
(2)此实验证明菠菜中含有Fe2+.
(3)请猜测一下在丙中加入稀硝酸的作用是把亚铁离子氧化成铁离子.
8.2016年诺贝尔化学奖揭晓,三位科学家分享该奖,以表彰他们在“合成分子机器”方面的研究.分子机器,指由分子尺度的物质构成、能使某种加工功能的机器,其构建主要是蛋白质.蛋白质从物质分类的角度应属于( )
| A. | 氧化物 | B. | 非金属单质 | C. | 盐 | D. | 有机物 |
12.核外电子数相同,核内质子数不同的两种粒子,它们不可能是( )
| A. | 一种元素的原子和另一种元素的离子 | |
| B. | 同种元素的原子和离子 | |
| C. | 一个物质的分子和离子 | |
| D. | 两种不同元素的离子 |
13.下列各组物质按单质、氧化物、混合物的顺序排列的是( )
| A. | 水、干冰、盐酸溶液 | B. | 红磷、纯碱、石油 | ||
| C. | 氧气、生石灰、天然气 | D. | 金刚石、熟石灰、空气 |
 原子、分子、离子都是构成物质的微观离子,如图所示是构成物质的粒子之间的关系:
原子、分子、离子都是构成物质的微观离子,如图所示是构成物质的粒子之间的关系: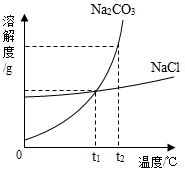 1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:①NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl ②2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑试回答下列问题:
1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:①NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl ②2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑试回答下列问题: