题目内容
1.小青按如图所示操作进行酸碱中和反应的实验,回答问题
(1)图E是稀释浓硫酸的操作示意图,甲烧杯中的物质应是浓硫酸.
(2)小青观察到图C中溶液由红色变为无色,认为氢氧化钠与硫酸恰好完全反应,化学方程式是2NaOH+H2SO4=Na2SO4+2H2O.
(3)小楚想用紫色石蕊溶液、氧化铜粉末、碳酸钠溶液、氯化钡溶液进一步确定反应后的无色溶液中溶质的成分,其中不能达到目的是氯化钡溶液.
分析 (1)根据浓硫酸的稀释方法分析解答即可;
(2)根据氢氧化钠和硫酸反应产生硫酸钠和水写出反应的方程式;
(3)要确定反应后的无色溶液中溶质的成分就是验证氢氧化钠和硫酸反应后的溶液中是否硫酸,也就是验证是否有氢离子.
解答 解:(1)浓硫酸溶于水会放出大量的热,水的密度比浓硫酸的密度小,所以如果将水倒入浓硫酸中水会浮在浓硫酸的液面上而沸腾造成液滴飞溅.故稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,所以烧杯中液体A是浓硫酸;故答案为:浓硫酸;
(2)氢氧化钠和硫酸反应产生硫酸钠和水;故填:2NaOH+H2SO4=Na2SO4+2H2O;
(3)氢离子会使紫色的石蕊试液变红,可以验证是否有氢离子;氧化铜能够和稀硫酸反应,验证硫酸的存在;碳酸钠能够和硫酸反应,验证硫酸的存在;氯化钡能够和硫酸及硫酸钠反应,因此不能确定硫酸的存在,因此不能达到目的是氯化钡溶液;故填:氯化钡溶液.
点评 本题考查了氢氧化钠和硫酸的中和反应,设计实验证明反应是否恰好完全进行,完成此题,可以依据课本已有的知识.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
11.浩瀚大海给我们提供很多资源,海水中含有大量氯化钠,工业上可以用氯化钠原料来制取碳酸钠、氢氧化钠、氯气和盐酸等.
(1)氢氧化钠溶液和碳酸钠溶液都能使酚酞变红色,它们的溶液pH>(填“<”、“=”或“>”)7.写出碳酸钠与石灰乳反应制备烧碱的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(2)试管中内壁残留下列物质,用盐酸浸泡能除去的是ACD.
A.铁锈锈渍 B.用碳粉还原氧化铜附着的红色固体
C.长时间盛放石灰水留下的白色固体 D.氢氧化钠和硫酸铜反应后的留下的蓝色固体
(3)工业上把浓海水除钙后,再加入碱性沉淀剂可以制备氢氧化镁.若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度.
某研究小组在控制反应温度是20~25℃和浓海水质量为1109g不变的条件下,进行下述对比实验,数据如下:
①进行实验a和b的目的是探究相同条件下,碳酸钠加入量对钙除去率的影响.
②搅拌速率越快,反应时间越长则消耗能源越多.为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件.在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是AC(填选项).
A.200r/min,3.5h B.200r/min,4.5h C.175r/min,4h D.225r/min,4h.
(1)氢氧化钠溶液和碳酸钠溶液都能使酚酞变红色,它们的溶液pH>(填“<”、“=”或“>”)7.写出碳酸钠与石灰乳反应制备烧碱的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(2)试管中内壁残留下列物质,用盐酸浸泡能除去的是ACD.
A.铁锈锈渍 B.用碳粉还原氧化铜附着的红色固体
C.长时间盛放石灰水留下的白色固体 D.氢氧化钠和硫酸铜反应后的留下的蓝色固体
(3)工业上把浓海水除钙后,再加入碱性沉淀剂可以制备氢氧化镁.若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度.
某研究小组在控制反应温度是20~25℃和浓海水质量为1109g不变的条件下,进行下述对比实验,数据如下:
| 实验 | 碳酸钠加入量/g | 搅拌速度r/min | 反应时间/h | 钙除去率/% |
| a | 1.78 | 200 | 3 | 44.8 |
| b | 2.32 | 200 | 3 | 60.2 |
| c | 2.32 | 125 | 4 | 55.1 |
| d | 2.32 | 200 | 4 | 64.6 |
②搅拌速率越快,反应时间越长则消耗能源越多.为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件.在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是AC(填选项).
A.200r/min,3.5h B.200r/min,4.5h C.175r/min,4h D.225r/min,4h.
12.下列物质中含有氧分子的是( )
| A. | 液氧 | B. | 水 | C. | 氧化汞 | D. | 二氧化碳 |
9.符合下列转化关系的物质甲是( )

| A. | Zn | B. | MgO | C. | Fe2O3 | D. | CuO |
16.对联是中国传统文化的瑰宝之一,下列对联中单从字面意义看包含化学变化的是( )
| A. | 上联:冰冻兵船 兵打冰 冰开兵出 下联:尼姑泥鞋 尼洗泥 泥落尼归 | |
| B. | 上联:此木为柴山山出 下联:因火成烟夕夕多 | |
| C. | 上联:水陆洲 洲停舟 舟行洲不行 下联:天心阁 阁落鸽 鸽飞阁未飞 | |
| D. | 上联:水中冻冰 冰种雪 雪上加霜 下联:空中腾雾 雾成云 云开见日 |
6.下列有关水的叙述中,正确的是( )
| A. | 用明矾溶液可以区分硬水和软水 | |
| B. | 净水操作中,相对净水程度最高的是蒸馏 | |
| C. | 加活性炭吸附的净水方式可以降低水的硬度 | |
| D. | 通过过滤的方法可以将水中所有杂质与水分离开来 |
13.下列变化属于化学变化的是( )
| A. | 酸雨腐蚀建筑物 | B. | 太阳能电池发电 | C. | 酒精挥发 | D. | 水的 天然循环 |
10.根据下列粒子结构示意图所获取的信息,正确的是( )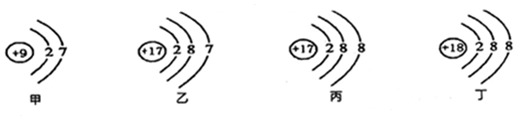

| A. | 甲、乙的化学性质相似 | B. | 乙、丙属于同种元素 | ||
| C. | 丙表示的是阳离子 | D. | 丁表示的元素属于金属元素 |
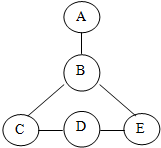 已知A~E是初中化学中常见的物质,它们之间的关系如图所示,相互之间的连线表示能发生化学反应.已知D是一种碱;C与E物质类别不同,且C是汽车用铅蓄电池的填充物质;B与E发生置换反应;A与B反应时火星四射.C的化学式是H2SO4; A物质具有的用途是供给呼吸(写一种即可);写出D与E反应的化学方程式2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
已知A~E是初中化学中常见的物质,它们之间的关系如图所示,相互之间的连线表示能发生化学反应.已知D是一种碱;C与E物质类别不同,且C是汽车用铅蓄电池的填充物质;B与E发生置换反应;A与B反应时火星四射.C的化学式是H2SO4; A物质具有的用途是供给呼吸(写一种即可);写出D与E反应的化学方程式2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.