题目内容
实验是学习化学的重要手段,通过实验可以培养实践能力和创新精神.(一)实验室制取气体是初中重要的一组实验,结合下列实验装置图回答有关问题:
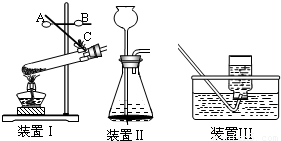
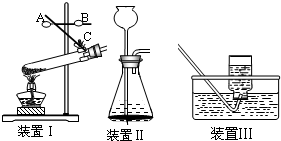
(1)装置 I是加热固体的装置,指出其中的错误______;要改正错误需要操作的按钮时______(填字母).
(2)使用装置 II制取O2,化学方程式为______ 2H2O+O2↑
【答案】分析:(一)(1)固体加热时试管应略微向下倾斜.
(2)II是固液制气的发生装置,据此回答问题即可.
(3)该装置一般是采用液封法进行气密性的检验.
(4)利用III装置收集气体要保证该气体不易溶于水.
(5)实验室若用锌和稀盐酸制取氢气时,因盐酸易挥发,所以制得的氢气内混有少量HCl气体和水蒸气,欲得到纯净、干燥的H2,必须除掉HCl气体和水蒸气.
(6)利用反应前后减小的是氧化铜中的氧,对氧化铜的质量进行计算.
(7)玻璃管中的水蒸气全部被E吸收,并且E还吸收了部分空气中的水,使E增加的质量变大;
解答:解:
(1)固体加热时试管应略微向下倾斜,否则容易炸裂试管.
(2)II是固液制气的发生装置,制取氧气是双氧水与二氧化锰的反应是固液制气型.
(3)该装置一般是采用液封法进行气密性的检验,及切断与外界的联通向长颈漏斗中注水,观看液面的变化.
(4)利用III装置收集气体要保证该气体不易溶于水,氢气氧气一氧化碳均不易溶于水.
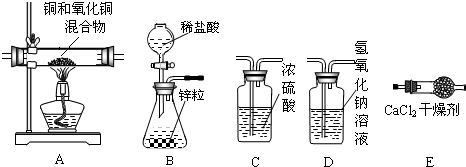
(5)验室若用锌和稀盐酸制取氢气时,因盐酸易挥发,所以制得的氢气内混有少量HCl气体和水蒸气,欲得到纯净、干燥的H2,必须先用装置D除掉HCl气体再用装置C除掉水蒸气后用装置E收集(氢气密度最小),因为装置D内盛的是氢氧化钠溶液能很快吸收HCl气体发生化学反应.
(6)反应前后固体的质量差是2.5g-2.1g=0.4g,则氧化铜的质量是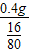 =2g,氧化铜的质量分数为
=2g,氧化铜的质量分数为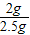 ×100%=80%
×100%=80%
(7)在高温条件下,玻璃管中的水蒸气全部被E吸收,并且E还吸收了部分空气中的水,使E增加的质量变大,从而使计算出的结果和实际值相比将偏大.
故答案为:(1)试管口向上倾斜(或试管口没有略向下倾斜) AB
(2)2H2O2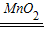 2H2O+O2↑
2H2O+O2↑
(3)夹紧装置中导管的橡胶管,在长颈漏斗中加少量水,长颈漏斗中的水保持不下去
(4)H2、O2、CO (5)D→C→A (6)80% (7)增大.
点评:此题是化学实验基本操作与综合应用考查题,解题时要对常规的实验有明确的认识,并且能对综合实验的问题进行深入的探讨.(二)是典型的实验探究题,熟练掌握氢气还原氧化铜的性质和实验才能准确解答该题,要分析清楚每步实验的目的即可准确解答该题.
(2)II是固液制气的发生装置,据此回答问题即可.
(3)该装置一般是采用液封法进行气密性的检验.
(4)利用III装置收集气体要保证该气体不易溶于水.
(5)实验室若用锌和稀盐酸制取氢气时,因盐酸易挥发,所以制得的氢气内混有少量HCl气体和水蒸气,欲得到纯净、干燥的H2,必须除掉HCl气体和水蒸气.
(6)利用反应前后减小的是氧化铜中的氧,对氧化铜的质量进行计算.
(7)玻璃管中的水蒸气全部被E吸收,并且E还吸收了部分空气中的水,使E增加的质量变大;
解答:解:
(1)固体加热时试管应略微向下倾斜,否则容易炸裂试管.
(2)II是固液制气的发生装置,制取氧气是双氧水与二氧化锰的反应是固液制气型.
(3)该装置一般是采用液封法进行气密性的检验,及切断与外界的联通向长颈漏斗中注水,观看液面的变化.
(4)利用III装置收集气体要保证该气体不易溶于水,氢气氧气一氧化碳均不易溶于水.
(5)验室若用锌和稀盐酸制取氢气时,因盐酸易挥发,所以制得的氢气内混有少量HCl气体和水蒸气,欲得到纯净、干燥的H2,必须先用装置D除掉HCl气体再用装置C除掉水蒸气后用装置E收集(氢气密度最小),因为装置D内盛的是氢氧化钠溶液能很快吸收HCl气体发生化学反应.
(6)反应前后固体的质量差是2.5g-2.1g=0.4g,则氧化铜的质量是
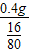 =2g,氧化铜的质量分数为
=2g,氧化铜的质量分数为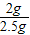 ×100%=80%
×100%=80%(7)在高温条件下,玻璃管中的水蒸气全部被E吸收,并且E还吸收了部分空气中的水,使E增加的质量变大,从而使计算出的结果和实际值相比将偏大.
故答案为:(1)试管口向上倾斜(或试管口没有略向下倾斜) AB
(2)2H2O2
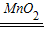 2H2O+O2↑
2H2O+O2↑(3)夹紧装置中导管的橡胶管,在长颈漏斗中加少量水,长颈漏斗中的水保持不下去
(4)H2、O2、CO (5)D→C→A (6)80% (7)增大.
点评:此题是化学实验基本操作与综合应用考查题,解题时要对常规的实验有明确的认识,并且能对综合实验的问题进行深入的探讨.(二)是典型的实验探究题,熟练掌握氢气还原氧化铜的性质和实验才能准确解答该题,要分析清楚每步实验的目的即可准确解答该题.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目