题目内容
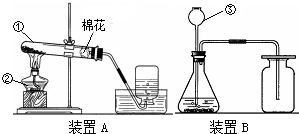
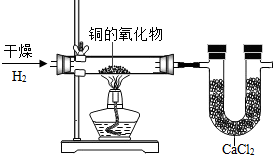 如图是分析一种化合物组成的实验装置.
如图是分析一种化合物组成的实验装置.实验结果如下:
| 实验前 | 实验后 | |
| 铜的氧化物+玻璃管 | 137.8g | 131.4g |
| 氯化钙+U形管 | 100.8g | 108.0g |
试根据实验数据求:
(1)完全反应后生成水的质量为
(2)生成的水中氧元素的质量为
(3)铜的氧化物中铜元素的质量为
(4)铜的氧化物中铜元素和氧元素的质量比为
(5)铜的氧化物中铜、氧原子个数的最简整数比为
(6)写出铜的氧化物的化学式:
考点:氢气的化学性质与燃烧实验,常见气体的检验与除杂方法,化学式的书写及意义
专题:氧气、氢气的性质与用途
分析:根据铜的氧化物减少的质量即被夺走得氧元素的质量,即是生成的水中所含氧元素的质量;而氯化钙增加的质量就是吸收的生成的水的质量进行解答.
解答:解:(1)完全反应生成的水,由于被干燥剂氯化钙所吸收,因此水的质量为:108.0g-100.8g═7.2g;
(2)由于水的质量为7.2g,所以水中氧元素的质量:7.2g×
×100%=6.4g;
(3)铜的氧化物中氧元素就是生成的水中氧元素的,所以铜元素的质量:137.8g-80.2g-6.4g=51.2g;
(4)铜的氧化物中有氧元素6.4g,铜元素51.2g,因此铜、氧元素的质量比为:51.2g:6.4g=8:1;
(5)可以根据元素的质量比直接求元素的原子个数比,氧化物中铜、氧元素的原子个数比为:
:
=2:1;
(6)铜的氧化物中铜、氧元素的原子个数比为2:1,该铜的氧化物的化学式为:Cu2O.
故答案为:
(1)7.2;(2)6.4;(3)51.2;(4)8:1; (5)2:1;(6)Cu2O.
(2)由于水的质量为7.2g,所以水中氧元素的质量:7.2g×
| 16 |
| 18 |
(3)铜的氧化物中氧元素就是生成的水中氧元素的,所以铜元素的质量:137.8g-80.2g-6.4g=51.2g;
(4)铜的氧化物中有氧元素6.4g,铜元素51.2g,因此铜、氧元素的质量比为:51.2g:6.4g=8:1;
(5)可以根据元素的质量比直接求元素的原子个数比,氧化物中铜、氧元素的原子个数比为:
| 8 |
| 64 |
| 1 |
| 16 |
(6)铜的氧化物中铜、氧元素的原子个数比为2:1,该铜的氧化物的化学式为:Cu2O.
故答案为:
(1)7.2;(2)6.4;(3)51.2;(4)8:1; (5)2:1;(6)Cu2O.
点评:主要根据实验来确定化合物的组成,考查了对化学式的有关计算,培养学生的理解能力和计算能力.

练习册系列答案
相关题目
质量相同的下列物质在氧气中燃烧,消耗氧气最少的是( )
| A、C | B、H2 |
| C、S | D、P |
 表示的是(填名称)
表示的是(填名称)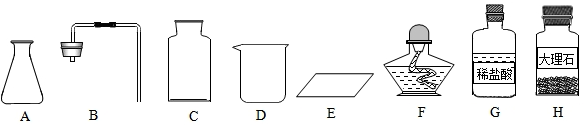
 实验室常用于制取氧气的方法有:
实验室常用于制取氧气的方法有: