题目内容
已知:在相同温度和相同体积的条件下,气体压强(P)与气体分子数目(N)成正比关系(P=kN).20℃时,若ag碳和bg氧气放入一体积不变的密闭容器中,测得容器内的气体压强为P,然后,提供一定条件使容器内的物质充分发生反应,待温度复原后,测得容器内的压强仍然为P,则a与b的关系是( )
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
考点:碳的化学性质,根据化学反应方程式的计算
专题:碳单质与含碳化合物的性质与用途
分析:由于反应前后容器内气体压强不变,根据在相同温度和相同体积的条件下,气体压强(P)与气体分子数目(n)成正比关系(P=kn),可判断反应前后气体的分子数目没改变;根据碳在氧气中充分燃烧与不充分燃烧的规律,此时碳应充分燃烧全部生成二氧化碳,其中氧气足量或过量;根据碳在氧气中完全燃烧的化学方程式,由反应中碳与所消耗氧气的质量关系,判断密闭容器中ag碳和bg氧气的关系.
解答:解:根据题意,反应前后分子数目不变,由C+O2
CO2与2C+O2
2CO,可判断碳在氧气中充分燃烧生成二氧化碳,
假设ag碳和bg氧气恰好完全反应,则
C+O2
CO2
12 32
ag bg
=
a=
,若容器中氧气有剩余,反应前后分子数目也不变,反应前后压强也相同,因此,容器中碳的质量a≤
故选D.
| ||
| ||
假设ag碳和bg氧气恰好完全反应,则
C+O2
| ||
12 32
ag bg
| 12 |
| ag |
| 32 |
| bg |
a=
| 3b |
| 8 |
| 3b |
| 8 |
故选D.
点评:根据碳在氧气中完全燃烧与不完全燃烧前后气体的分子个数关系,判断该题中所发生反应为完全燃烧生成二氧化碳,是解决问题的关键.

练习册系列答案
相关题目
下列物质久置于空气中质量都会改变,其原因只和水蒸气有关的是( )
| A、澄清石灰水 | B、浓硫酸 |
| C、生石灰 | D、洁净的铁钉 |
在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:关于此反应的认识不正确的是( )
| 物质 | W | G | H | P |
| 反应前质量/g | 18 | 1 | 2 | 32 |
| 反应后质量/g | 待测 | 26 | 2 | 12 |
| A、物质H一定是该反应的催化剂 |
| B、该反应一定是化合反应 |
| C、W、P是反应物 |
| D、待测值为13 |
如图是元素周期表中第三周期元素的原子结构示意图:
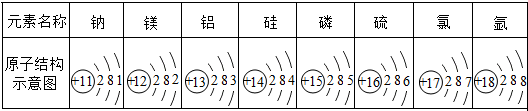
依据如图判断,下列结论正确的是( )

依据如图判断,下列结论正确的是( )
| A、12 号元素的原子,在化学反应中容易得到电子变成离子 |
| B、钠元素与硫元素形成化合物的化学式为Na2S |
| C、第三周期元素的化学性质相似 |
| D、Cl→Cl-,则 Cl 核内有 18 个质子 |
下列试剂中,能把NaOH溶液、稀硫酸、CaCl2溶液一次鉴别出来的是( )
| A、KCl溶液 |
| B、K2CO3溶液 |
| C、NaNO3溶液 |
| D、稀盐酸 |
