题目内容
将10g不纯的锌粒(杂质不容与水也不与酸反应)及足量的稀硫酸投入到烧杯中,称得质量为110g,恰好完全反应后再次称量烧杯总质量为109.8g.试计算:
(1)反应生成的氢气的质量为 ;
(2)锌粒中纯锌的质量分数.
(1)反应生成的氢气的质量为
(2)锌粒中纯锌的质量分数.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据质量守恒定律生成氢气的质量就等于反应器物质的总质量减去反应后物质的总质量解答;
(2)利用锌与稀硫酸反应的化学方程式和生成氢气的质量,列出比例式,就可计算出锌粒中纯锌的质量,然后就可求出锌粒中纯锌的质量分数.
(2)利用锌与稀硫酸反应的化学方程式和生成氢气的质量,列出比例式,就可计算出锌粒中纯锌的质量,然后就可求出锌粒中纯锌的质量分数.
解答:解:(1)生成氢气的质量为110g-109.8g=0.2g;
(2)设锌粒中纯锌的质量为x
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
=
x=6.5g
锌粒中纯锌的质量分数为
×100%=65%
答:锌粒中纯锌的质量分数为65%.
(2)设锌粒中纯锌的质量为x
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.2g
| 65 |
| x |
| 2 |
| 0.2g |
x=6.5g
锌粒中纯锌的质量分数为
| 6.5g |
| 10g |
答:锌粒中纯锌的质量分数为65%.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
原子核外第三电子层与第一电子层的电子数相等的原子,其质子数为( )
| A、20 | B、14 | C、12 | D、10 |
下列化学方程式书写正确的是( )
| A、4P+5O2═2P2O5 | ||||
B、C+O2
| ||||
C、Mg+O2
| ||||
D、2H2O2
|
下列四种变化中,属于物理变化是( )
| A、植物呼吸 |
| B、食物腐败 |
| C、利用空气中氮气制氮肥 |
| D、分离液态空气制取氧气 |
铁钉在钉入木制品时,有经验的木匠习惯用口水将铁钉润湿,你认为这样做的主要目的是( )
| A、使铁钉更容易钉入木制品 |
| B、这是为了使铁钉更易生锈,防止脱落 |
| C、这是为了防止铁钉生锈而腐蚀 |
| D、增大钉入时的摩擦力 |
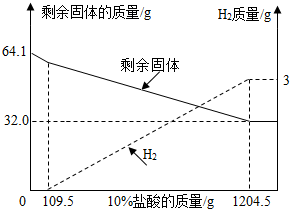 小亮同学对在空气中放置一段时间的“铜树”(铝丝浸泡在硫酸铜溶液中制成,如图)的成分进行分析,取出64.1g固体样品,用10%的盐酸充分溶解,溶液呈无色,产生的气体和剩余固体随消耗10%的盐酸质量变化关系曲线如图:
小亮同学对在空气中放置一段时间的“铜树”(铝丝浸泡在硫酸铜溶液中制成,如图)的成分进行分析,取出64.1g固体样品,用10%的盐酸充分溶解,溶液呈无色,产生的气体和剩余固体随消耗10%的盐酸质量变化关系曲线如图: