题目内容
10.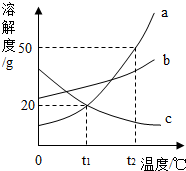 a、b、c三种固体物质的溶解度曲线如图所示,下列叙述正确的是( )
a、b、c三种固体物质的溶解度曲线如图所示,下列叙述正确的是( )| A. | a物质的溶解度大于b物质的溶解度 | |
| B. | t1℃时,a、c两种物质形成的溶液中溶质的质量分数相等 | |
| C. | t2℃时,30ga物质加入50g水中得到80g溶液 | |
| D. | t2℃时,c物质的饱和溶液升温会有晶体析出 |
分析 根据已有的溶解度曲线结合其意义进行分析解答即可.
解答 解:A、比较溶解度需要在一定的温度下比较,错误;
B、t1℃时,a、c两种物质形成的饱和溶液中溶质的质量分数相等,错误;
C、t2℃时,30ga物质加入50g水中,能溶解a物质的质量为:$\frac{50g}{100g}×50g$=25g,得到75g溶液,错误;
D、t2℃时,c物质的饱和溶液升温会有晶体析出,正确;
故选D.
点评 掌握溶解度曲线的意义是正确解答本题的关键.

练习册系列答案
相关题目
1.我们生活在物质世界里,下列叙述中不涉及化学变化的是( )
| A. | 不纯的氢气燃烧发生爆炸 | B. | 涂在墙上的熟石灰逐渐变硬 | ||
| C. | 焦炭冶炼金属 | D. | 舞台上用干冰制造“云雾” |
5.常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反虚后的产物.
(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是Fe3O4.
【实验探究】
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3是红棕色粉末.
【总结与归纳】由上述实验得出比较金属活动性强弱的方法有:
①金属是否可以与酸反应置换出氢气;②金属是否可以与水反应置换出氢气.

(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是Fe3O4.
【实验探究】
| 实验操作 | 实验现象及结论 |
【总结与归纳】由上述实验得出比较金属活动性强弱的方法有:
①金属是否可以与酸反应置换出氢气;②金属是否可以与水反应置换出氢气.
2.通过下列实验操作和现象能得出相应结论的是( )
| A | B | C | D | |
| 实验 操作 | 把燃着的木条插入某瓶无色气体中 |  | 将白磷浸没在热水中,再向热水中的白磷通氧气 |  |
| 现象 | 木条熄灭 | 放置一周后,A中铁钉生锈,B中铁钉无明显变化 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 放置一段时间,长颈漏斗中水面下降 |
| 结论 | 瓶中的气体是二氧化碳 | 铁生锈需要氧气和水 | 氧气是燃烧需要的条件之一 | 装置气密性良好 |
| A. | A | B. | B | C. | C | D. | D |
20.实验室部分装置如图所示,请回答下列问题.

(1)请选择制取氧气的发生装置和收集装置,填写在如表中(填字母).
(2)实验室用高锰酸钾制取氧气的文字表达式是高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(3)如果用F装置收集氧气,导管口开始有气泡放出时,不宜立即收集的原因是刚开始放出的气体不纯,当气泡均匀并连续地放出时,再收集,验满的方法是集气瓶口有大量气泡冒出.
(4)实验室用过氧化氢制取氧气的文字表达式是过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,
(5)使用装置B的优点是不加热,操作简单;或不加热,节约能源;或便于添加液体等(答一点).

(1)请选择制取氧气的发生装置和收集装置,填写在如表中(填字母).
| 选用药品 | 发生装置 | 收集装置 |
| H2O2溶液、MnO2 | B | D或F |
| KMnO4 | A |
(3)如果用F装置收集氧气,导管口开始有气泡放出时,不宜立即收集的原因是刚开始放出的气体不纯,当气泡均匀并连续地放出时,再收集,验满的方法是集气瓶口有大量气泡冒出.
(4)实验室用过氧化氢制取氧气的文字表达式是过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,
(5)使用装置B的优点是不加热,操作简单;或不加热,节约能源;或便于添加液体等(答一点).
 e.
e.
 如图是电解水的简易装置.
如图是电解水的简易装置.