题目内容
10.电石气是一种中重要的化工原料,工业生产电石气的反应原理是:CaC2+2H2O═Ca(OH)2+X↑试确定电石气X的化学式是( )| A. | C2H2O | B. | CH4 | C. | C2H2 | D. | CH2 |
分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
解答 解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式CaC2+2H2O═Ca(OH)2+X↑,反应前钙、碳、氢、氧原子个数分别为1、2、4,2,反应后的生成物中钙、碳、氢、氧原子个数分别是1、0、2、2,根据反应前后原子种类、数目不变,则每个X分子由2个碳原子和2个氢原子构成,则物质X的化学式为C2H2.
故选:C.
点评 本题难度不大,利用化学反应前后原子守恒来确定物质的化学式是正确解答此类题的关键.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
1.下列物质中,属纯净物又属单质的是( )
| A. | 水 | B. | 煤 | C. | 金属铁 | D. | 食盐水 |
20.下列实验方案中,合理的是( )
| A. | 除去二氧化碳中混有的少量一氧化碳:点燃混合气体 | |
| B. | 在实验室里制取纯净的二氧化碳:用木炭在氧气中燃烧 | |
| C. | 除去氧气中混有的二氧化碳:将混合气体通过足量的石灰水 | |
| D. | 证明集气瓶中盛有的是二氧化碳:将燃着的木条伸入集气瓶中 |
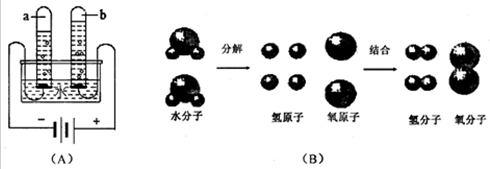




 ,用化学符号表示下列微粒:
,用化学符号表示下列微粒: