题目内容
11.下列有关糖类物质说法正确的是( )| A. | 都由碳、氧、氧三种元素组成 | B. | 所有糖类都有甜味 | ||
| C. | 只有光合作用才能形成葡萄糖 | D. | 都能被人体消化吸收 |
分析 A、糖类由C、H、O三种元素组成;
B、多糖本身无甜味;
C、暗反应的产物可以是糖类;
D、淀粉属于高分子化合物,在相应酶的作用下水解成可以被人体吸收的小分子物质.人体内没有纤维素酶,不能消化吸收纤维素
解答 解:A、糖类由C、H、O三种元素组成,正确;
B、单糖、二塘多有甜味,但多糖本身无甜味,故B错误.
C、暗反应的产物可以是糖类,错误;
D、膳食纤维是指除淀粉以外较复杂糖类物质,包括纤维素和果胶等,这些复杂的糖类物质人体是不能消化吸收的,错误.
故选A
点评 本题考查糖类的元素组成,题目难度不大.熟练掌握人体需要的主要的六大类营养物质.关键点:膳食纤维是人体的“第七类营养素”,不能消化.

练习册系列答案
相关题目
5.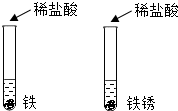 为了探究盐酸除铁锈的实验中,气体是由什么产生的,设计如下实验:(1)在两支试管分别放入铁粉和铁锈;(2)分别加入等量等浓度的稀盐酸,观察现象.针对该实验的目的,下列评价或改进正确的是( )
为了探究盐酸除铁锈的实验中,气体是由什么产生的,设计如下实验:(1)在两支试管分别放入铁粉和铁锈;(2)分别加入等量等浓度的稀盐酸,观察现象.针对该实验的目的,下列评价或改进正确的是( )
 为了探究盐酸除铁锈的实验中,气体是由什么产生的,设计如下实验:(1)在两支试管分别放入铁粉和铁锈;(2)分别加入等量等浓度的稀盐酸,观察现象.针对该实验的目的,下列评价或改进正确的是( )
为了探究盐酸除铁锈的实验中,气体是由什么产生的,设计如下实验:(1)在两支试管分别放入铁粉和铁锈;(2)分别加入等量等浓度的稀盐酸,观察现象.针对该实验的目的,下列评价或改进正确的是( )| A. | 该实验步骤正确完整 | |
| B. | 应补充一个铁与水反应的实验 | |
| C. | 应补充一个铁锈与水反应的实验 | |
| D. | 应补充一个铁锈与水反应的实验和补充一个铁与水反应的实验 |
6. 如图是A、B、C三种物质的溶解度曲线图,下列说法不正确的是( )
如图是A、B、C三种物质的溶解度曲线图,下列说法不正确的是( )
 如图是A、B、C三种物质的溶解度曲线图,下列说法不正确的是( )
如图是A、B、C三种物质的溶解度曲线图,下列说法不正确的是( )| A. | 三种物质的溶解度大小为SA>SB>SC | |
| B. | 三种物质中溶解度受温度影响最大的是A | |
| C. | M点表示在t2℃时,A物质的溶解度为80g | |
| D. | N点表示在t1℃时,A、B、C三种物质饱和溶液溶质质量分数都为28.6% |
16.某校化学小组对热水壶底部水垢的主要成分进行了如下探究,请完成以下活动并回答相关问题.
【查阅资料】
天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见下表(20℃):
根据上述物质的溶解性,小组同学确定水垢的主要成分中一定含有的两种物质是,可能含有Ca(OH)2和MgCO3.
【提出问题】水垢的主要成分中是否含有Ca(OH)2和MgCO3呢?
【实验方案1】确定水垢中是否含Ca(OH)2
【实验方案2】确定水垢中是否含MgCO3
利用下列实验装置,完成实验2探究.其主要实验步骤如下:
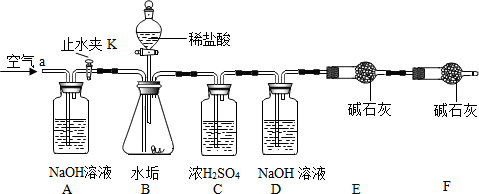
按如图组装后,将9.8g水垢试样放入锥形瓶中,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后精确称量D、E装置总质量为600.0g关闭止水夹K,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处再次缓缓鼓入空气,一段时间后称量装置D、E的总质量为604.4g(注意:碱石灰主要成分为CaO和NaOH的混合物).
【实验讨论】
(1)加入药品前应;待锥形瓶中不再产生气泡时,打开止水夹K,缓缓鼓入空气的目的是.
(2)C装置的作用是:干燥生成的气体.
(3)装置 B中生成CO2的质量为4.4g.通过计算说明该水垢中(填序号)含MgCO3.
A.一定B.一定不C.可能D.无法确定
【实验方案3】定量探究水垢中氢氧化镁的质量分数
另取质量为9.8g的水垢试样,加入7.3%稀盐酸与之恰好完全反应,测得消耗稀盐酸110g.结合以上数据和实验结论,计算水垢样品中氢氧化镁的质量分数(写出计算过程,结果保留1位小数).
【反思】缺少F装置会使所测水垢样品中氢氧化镁的质量分数偏小(填写“偏大”或“偏小”或“不变”).
【查阅资料】
天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见下表(20℃):
| 阴离子 阳离子 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
【提出问题】水垢的主要成分中是否含有Ca(OH)2和MgCO3呢?
【实验方案1】确定水垢中是否含Ca(OH)2
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液. | 无白色沉淀 | 水垢中无Ca(OH)2 |
利用下列实验装置,完成实验2探究.其主要实验步骤如下:

按如图组装后,将9.8g水垢试样放入锥形瓶中,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后精确称量D、E装置总质量为600.0g关闭止水夹K,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处再次缓缓鼓入空气,一段时间后称量装置D、E的总质量为604.4g(注意:碱石灰主要成分为CaO和NaOH的混合物).
【实验讨论】
(1)加入药品前应;待锥形瓶中不再产生气泡时,打开止水夹K,缓缓鼓入空气的目的是.
(2)C装置的作用是:干燥生成的气体.
(3)装置 B中生成CO2的质量为4.4g.通过计算说明该水垢中(填序号)含MgCO3.
A.一定B.一定不C.可能D.无法确定
【实验方案3】定量探究水垢中氢氧化镁的质量分数
另取质量为9.8g的水垢试样,加入7.3%稀盐酸与之恰好完全反应,测得消耗稀盐酸110g.结合以上数据和实验结论,计算水垢样品中氢氧化镁的质量分数(写出计算过程,结果保留1位小数).
【反思】缺少F装置会使所测水垢样品中氢氧化镁的质量分数偏小(填写“偏大”或“偏小”或“不变”).
3.下列变化中,有一种与其他三种本质不同,这种变化是( )
| A. | 水沸腾 | B. | 高压锅爆炸 | C. | 石蜡熔化 | D. | 食物腐烂 |
20.下列物质属于纯净物的是( )
| A. | 洁净的空气 | B. | 寒冷的干冰 | C. | 清澈的泉水 | D. | 新鲜的牛奶 |