题目内容
20.实验室进行CO2的制取实验,请回答下列问题:(1)药品的选择:实验记录如下:
| 实验序号 | 实验 | 实验现象 |
| A | 块状石灰石放入稀盐酸中 | 产生气泡速率适中 |
| B | 块状石灰石放入稀硫酸中 | 产生气泡速率缓慢,并逐渐停止 |
| C | 碳酸钠粉末放入稀盐酸中 | 产生气泡速率很快 |
(2)装置的选择:
a.如图仪器中,序号为⑤和⑩的名称为:集气瓶、水槽.
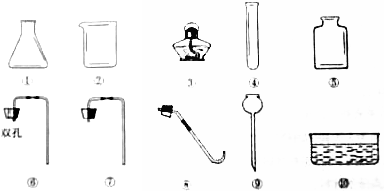
b.根据选择的药品和反应条件,组装一套实验室制取和收集二氧化碳气体的装置,应选择上图中的仪器是①⑤⑥⑨(填序号).
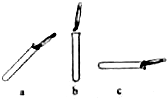
(3)制取和收集:图中,装入固体药品的操作正确的是C(填序号);采用向上排气法收集二氧化碳气体,利用它的密度比空气大性质.
(4)写出检验二氧化碳气体发生反应的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O.
分析 (1)根据制取气体的条件考虑;(2)a.熟记常见仪器的名称;b.制取二氧化碳用碳酸钙和稀盐酸,不需要加热,收集二氧化碳的方法是向上排空气法;(3)根据固体药品的取用方法考虑;因为二氧化碳的密度比空气密度大,所以用向上排空气法收集;(4)检验二氧化碳用澄清石灰水.
解答 解:(1)制取气体的反应物反应速度适中,有利于收集,不能太快和太慢,故选A;
(2)a.⑤是集气瓶,⑩是水槽;b.制取二氧化碳用碳酸钙和稀盐酸,反应物是固体和液体,不需要加热,收集二氧化碳的方法是向上排空气法;所以选择①⑤⑥⑨;
(3)装入固体药品的操作正确的是:先将试管横放,用镊子将药品放在试管口,再将试管竖起;采用向上排气法收集二氧化碳气体,利用它的密度比空气大的性质;
(4)检验二氧化碳用澄清石灰水,反应物是氢氧化钙和二氧化碳,生成物是碳酸钙和水,所以方程式是:Ca(OH)2+CO2=CaCO3↓+H2O;
故答案为:(1)A;(2)a.集气瓶;水槽;(3)C;密度比空气大;(4)Ca(OH)2+CO2=CaCO3↓+H2O.
点评 解答本题关键是要知道发生装置的选择与反应条件和反应物的状态有关,收集装置的选择与气体的性质和密度有关.

练习册系列答案
相关题目
10.下列有关溶解、溶液的说法中不正确的是( )
| A. | 用汽油、洗涤剂都能洗去油污,二者都是利用溶解作用 | |
| B. | 从5%的蔗糖溶液中取出1滴,这1滴溶液的浓度仍为5% | |
| C. | 酸、碱、盐的溶液能导电,是因为溶液中存在自由移动的离子 | |
| D. | 在配制溶液时,所用的溶质可以是固体、液体,也可以是气体 |
11.下列日常学习生活中的做法正确的是( )
| A. | 坚持只喝纯净水 | B. | 把浓硫酸倒入盛有水的量筒里稀释 | ||
| C. | 进入深洞时要带电筒还要打火把 | D. | 用亚硝酸钠代替食盐作调味品 |
8.生活中遇到的问题,常常涉及化学知识.下列说法中.不正确的是( )
| A. | 将青菜放入着火的油锅以降低其着火点 | |
| B. | 将用过的铁锅洗净擦干以防生锈 | |
| C. | 用加热煮沸的方法可降低水的硬度 | |
| D. | 用燃烧闻气味的方法可鉴别棉纤维和羊毛 |
15.甲、乙两化学兴趣小组用如图1所示的实验装置,通过测定产生相同体积氧气所用时间的长短来探究影响H2O2分解速率的因素.
(1)甲组:按如下设计的方案实验,请完成表1:
(2)乙组:按如下设计的方案实验,请完成表2:
(3)甲、乙两小组通过数次实验得出如图2所示的数据,请回答下列问题: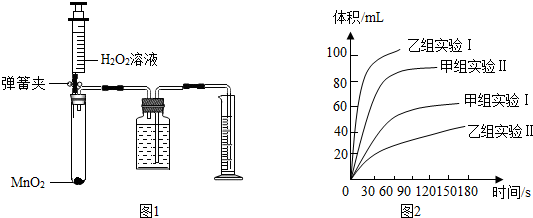
①从甲组实验得出的数据可知:H2O2浓度越大,分解速率越快.
②由乙组研究的影响H2O2分解因素的数据分析:相同条件下,H2O2在碱性(填“酸性”或“碱性”)环境下放出气体速率较快;写出H2O2分解的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O.
【发现问题】实验开始时,H2O2溶液的温度为25℃;实验结束时,溶液的温度明显升高.说明H2O2分解是放热(选填“放热”或“吸热”)反应.
【注意:若答对第(5)小题将奖励 4分,化学卷总分不超过60分】
【反思运用】同学们经过讨论、交流和网上搜资料,提出下面两种制取H2O2液的方 法:
①用Na2O2(过氧化钠)与 H2SO4溶液作反应物,反应时将温度控制在-5~+5℃范围,生成的Na2SO4,会以
Na2SO4•10H2O晶体的形式析出,反应原理为 Na2O2+H2S04+10H2O═NaSO4•10H2O+H20,制取时Na2O2的量不能过量,因为Na2O2与水反应会生成NaOH.若Na2O2过量会造成(在碱性环境中)生成的过氧化氢分解.
②用BaO2(过氧化鋇)与H2SO4溶液作反应物.在常温下就可反应生成H2O2,试写出反应的化学方程式BaO2+H2SO4=BaSO4↓+H2O2.方法“②”比方法“①”更易操作,理由是方法①要控制好反应的温度,才能使Na2SO4•10H2O晶体析出,而方法②生成的硫酸钡是沉淀,容易与过氧化氢溶液分离.
(1)甲组:按如下设计的方案实验,请完成表1:
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| Ⅰ | 探究溶液的浓度对H2O2分解速率的影响 | 25℃ | 0.2gMnO2 | 10mL 4%H2O2 |
| Ⅱ | 25℃ | 0.2gMnO2 | 10mL 8%H2O2 |
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 | 实验时溶液 酸碱度 |
| Ⅰ | 探究溶液的酸碱性 对H2O2分解速率的影响 | 25℃ | 0.2gMnO2 | 0mL 8%H2O2 | pH=10.0 |
| Ⅱ | 25℃ | 0.2gMnO2 | 0mL 8%O2 | pH=4.0 |

①从甲组实验得出的数据可知:H2O2浓度越大,分解速率越快.
②由乙组研究的影响H2O2分解因素的数据分析:相同条件下,H2O2在碱性(填“酸性”或“碱性”)环境下放出气体速率较快;写出H2O2分解的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O.
【发现问题】实验开始时,H2O2溶液的温度为25℃;实验结束时,溶液的温度明显升高.说明H2O2分解是放热(选填“放热”或“吸热”)反应.
【注意:若答对第(5)小题将奖励 4分,化学卷总分不超过60分】
【反思运用】同学们经过讨论、交流和网上搜资料,提出下面两种制取H2O2液的方 法:
①用Na2O2(过氧化钠)与 H2SO4溶液作反应物,反应时将温度控制在-5~+5℃范围,生成的Na2SO4,会以
Na2SO4•10H2O晶体的形式析出,反应原理为 Na2O2+H2S04+10H2O═NaSO4•10H2O+H20,制取时Na2O2的量不能过量,因为Na2O2与水反应会生成NaOH.若Na2O2过量会造成(在碱性环境中)生成的过氧化氢分解.
②用BaO2(过氧化鋇)与H2SO4溶液作反应物.在常温下就可反应生成H2O2,试写出反应的化学方程式BaO2+H2SO4=BaSO4↓+H2O2.方法“②”比方法“①”更易操作,理由是方法①要控制好反应的温度,才能使Na2SO4•10H2O晶体析出,而方法②生成的硫酸钡是沉淀,容易与过氧化氢溶液分离.
5.下列化肥中属于氮肥的是( )
| A. | 磷矿粉 | B. | 氯化钾 | C. | 过磷酸钙 | D. | 硫酸铵 |
3.ClO2是优良的饮用水消毒剂.ClO2中氯元素的化合价是( )
| A. | +5 | B. | +4 | C. | +2 | D. | -1 |
17.下列各组中,物质的俗称,学名与化学式表示同一物质的是( )
| A. | 酒精、乙醇、C2H5OH | B. | 小苏打、纯碱、NaOH | ||
| C. | 熟石灰、氧化钙、CaO | D. | 可燃冰、甲烷、CH4 |