题目内容
3.采用适当的试剂,可从石灰石(主要成分是CaCO3)中获得高纯度CaCO3,其流程如图:(流程中的杂质不溶于水也不与酸反应)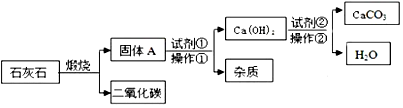
(1)流程图中进行的操作①的名称是过滤,该操作的温度要求控制在相对较低(填“较高”或“较低”)的环境下进行,才能更好地提高提纯效率.
(2)石灰石煅烧反应的基本反应类型是分解反应.
(3)该流程图所示物质中,溶于水放出大量热的氧化物是CaO(填“化学式”),该物质与水反应的化学方程式为CaO+H2O═Ca(OH)2.
(4)使原料中各原子的利用率尽可能达到100%是“绿色化学”的核心理念之一,上述流程中有的物质可以再利用,该流程中可再利用的物质是CO2和H2O.(填“化学式”).
分析 过滤能够把不溶于水的物质从液体中除去;石灰石煅烧过程中,碳酸钙分解生成氧化钙和二氧化碳;氧化钙溶于水放出大量的热,能和水反应生成氢氧化钙;实现物质的循环利用,可以节约能源,同时有利于保护环境.据此解答.
解答 解:(1)流程图中进行的操作①得到的是氢氧化钙溶液和杂质,故是过滤操作,氢氧化钙的溶解度随温度的升高而增大,故需要控制在较低的温度下进行,故填:过滤; 较低;
(2)石灰石煅烧反应生成氧化钙和二氧化碳,属于分解反应,故填:分解反应;
(3)该流程图中氧化钙与是反应生成氢氧化钙的过程中放出热量,故填:CaO;CaO+H2O═Ca(OH)2;
(4)上述流程中有的物质可以再利用,该流程中可循环利用的物质是H2O和CO2.故填:CO2; H2O.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
14.五光十色的霓虹灯把节日的夜晚妆点得分外美观.下列气体一般不可用于填充电灯泡的是( )
| A. | 氮气 | B. | 氧气 | C. | 氙气 | D. | 氖气 |
11.下列化学方程式书写正确的是( )
| A. | H2SO4+NaOH═NaSO4+H2O | B. | BaCO3+2HNO3═Ba(NO3)2+H2O+CO2↑ | ||
| C. | Ag+HCl═AgCl↓+H2↑ | D. | 2NaOH+K2CO3═2KOH+Na2CO3 |
8.小金同学根据如图所示实验分析得出的结论中,不正确的是( )
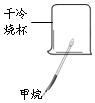 | 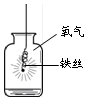 | 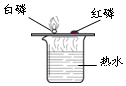 |  |
| A、甲烷燃烧生成二氧化碳和水 | B、铁能在氧气中燃烧 | C、白磷的着火点比红磷的低 | D、二氧化碳的密度比空气大,不燃烧也不支持燃烧 |
| A. | A | B. | B | C. | C | D. | D |
15.正确的实验操作是进行科学实验的重要保障.下列操作中,合理的是( )
| A. | 对试管内的液体加热时,试管口不能朝向有人的方向 | |
| B. | 稀释浓硫酸时,将水注入盛有浓硫酸的量筒中 | |
| C. | 测定某溶液的pH时,先用水将pH试纸润湿 | |
| D. | 用托盘天平称量氢氧化钠固体时,放在左盘的纸上称量 |
12.在一定条件下,向一密闭容器内加入A、B、C、D四种物质各20g,充分反应后测定其质量,得到数据如下表所示.下列判断中正确的是( )
①容器内发生了分解反应;
②容器内发生了化合反应;
③反应后容器内C的质量为16g;
④容器内发生的反应可能为B→C+D;
⑤反应过程中,物质B和D减少的质量比为5:3;
⑥若这个反应需要催化剂,则A可能是催化剂.
| 物 质 | A | B | C | D |
| 反应前质量(g) | 20 | 20 | 20 | 20 |
| 反应后质量(g) | 20 | 30 | 未知 | 14 |
②容器内发生了化合反应;
③反应后容器内C的质量为16g;
④容器内发生的反应可能为B→C+D;
⑤反应过程中,物质B和D减少的质量比为5:3;
⑥若这个反应需要催化剂,则A可能是催化剂.
| A. | ①③⑤⑥ | B. | ②③⑥ | C. | ②③④⑤⑥ | D. | ①④⑤⑥ |
13.下列叙述中可以用质量守恒定律解释的是( )
| A. | 20g水和30g酒精混合后质量为50g | |
| B. | 1t纯铁在高温下熔化为铁水,质量仍为1t | |
| C. | 稀盐酸滴入盛装碳酸钠粉末的烧杯中总质量减少了 | |
| D. | 某溶质质量分数为20%的溶液中含5g溶质和25g溶剂 |
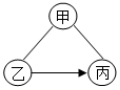 ①乙物质是Na2CO3或NaOH.
①乙物质是Na2CO3或NaOH.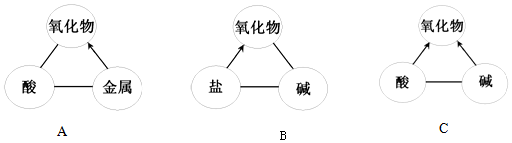
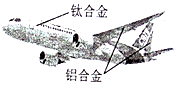 2017年5月5日,中国自制干线客机C919,从上海浦东机场徐徐起飞,自此开辟出一片属于中国航空工业的填空.结合所学化学知识,回答下列问题
2017年5月5日,中国自制干线客机C919,从上海浦东机场徐徐起飞,自此开辟出一片属于中国航空工业的填空.结合所学化学知识,回答下列问题