题目内容
16.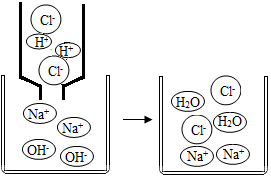 初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH-═H2O,如图,像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式,离子方程式的书写一般步骤如下:(以碳酸钠与氯化钙反应为例).
初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH-═H2O,如图,像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式,离子方程式的书写一般步骤如下:(以碳酸钠与氯化钙反应为例).①写出反应的化学方程式CaCl2+Na2CO3═2NaCl+CaCO3↓;
②把易溶于水,易电离的物质写出离子形式,把难溶的物质,气体和水等仍用化学式表示,上述方程式可改写成2Na++CO32-+Ca2++2Cl-═CaCO3↓+2Na++2Cl-;
③删除方程式两边不参加反应的粒子Ca2++CO32-→CaCO3↓
④检查方程式两边各元素的原子个数和电荷数是否相等,试回答:
(1)酸碱盐在水溶液中发生的复分解反应实质就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或沉淀或水生成,反应就能发生.
(2)写出稀盐酸滴在大理石上所发生反应的离子方程式CaCO3+2H+═Ca2++CO2↑+H2O;
(3)下列各组中的离子,能在溶液中大量共存的是D.
A、Na+、H+、SO42-、OH- B、Na+、Ca2+、CO32-、Cl-
C、Na+、H+、CO32-、Cl- D、K+、Cu2+、SO42-、Cl-
(4)写出一个能用Fe+2H+=Fe2++H2↑表示的化学方程式Fe+2HCl═FeCl2+H2↑.
分析 ①根据化学方程式的书写方法分析解答;
(1)根据复分解反应发生的条件来分析;
(2)根据离子方程式的书写方法进行分析.
(3)根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能大量共存,据此进行分析判断即可;
(4)根据复分解反应的实质进行分析.
解答 解:①碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠;故填:CaCl2+Na2CO3═2NaCl+CaCO3↓;
(1)酸碱盐在水溶液中发生的复分解反应实质就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或沉淀或水生成,反应就能发生.故填:沉淀或水;
(2)大理石的主要成分是碳酸钙,与稀盐酸反应生成氯化钙、水和二氧化碳,反应的离子方程式为CaCO3+2H+═Ca2++CO2↑+H2O;故填:CaCO3+2H+═Ca2++CO2↑+H2O;
(3)A.氢离子与氢氧根离子能结合成水,不能大量共存;
B.钙离子与碳酸根离子能结合成碳酸钙沉淀,不能大量共存;
C.氢离子与碳酸根离子能结合成二氧化碳气体与水,不能大量共存;
D.四种离子间不能结合成沉淀、气体或水,能大量共存.
故填:D;
(4)该离子方程式表示了单质铁与稀盐酸或稀硫酸反应生成氯化亚铁或硫酸亚铁与氢气;故填:Fe+2HCl═FeCl2+H2↑(答案合理即可).
点评 本题考查的是复分解反应的条件和复分解反应的实质,完成此题,可以依据已有的知识进行.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
7.央视《每周质量报告》本期节目《胶囊里的秘密》,曝光河北一些企业,用生石灰处理皮革废料,熬制成工业明胶,卖给绍兴新昌一些企业制成药用胶囊,最终流入药品企业,进入患者腹中.由于皮革在工业加工时,要使用含铬的鞣制剂,因此这样制成的胶囊,往往重金属铬超标.请问这里的“铬”是指( )
| A. | 铬元素 | B. | 铬单质 | C. | 铬原子 | D. | 铬离子 |
4.下列生活中的物质,属于氧化物的是( )
| A. | 可口可乐 | B. | 食盐 | C. | 双氧水 | D. | 食醋 |
11.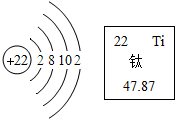 如图是钛元素的原子结构示意图和该元素在元素周期表中的单元格,下列说法不正确的是( )
如图是钛元素的原子结构示意图和该元素在元素周期表中的单元格,下列说法不正确的是( )
 如图是钛元素的原子结构示意图和该元素在元素周期表中的单元格,下列说法不正确的是( )
如图是钛元素的原子结构示意图和该元素在元素周期表中的单元格,下列说法不正确的是( )| A. | 该元素属于金属元素 | |
| B. | 该原子在化学变化中容易失去电子 | |
| C. | 该原子的相对原子质量为47.87g | |
| D. | 该原子的质量主要由构成其原子的质子和中子决定 |
1.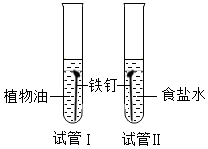 下列说法正确的是( )
下列说法正确的是( )
 下列说法正确的是( )
下列说法正确的是( )| A. | 乙醇、橡胶都属于合成高分子材料 | |
| B. | 蛋白质、糖类均属于基本营养素 | |
| C. | 如图试管Ⅰ中铁钉比试管Ⅱ中更容易绣蚀 | |
| D. | 物质由气态变成液态,分子间的间隔变大 |
16.下列实验操作正确的是( )
| A. | 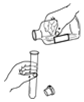 倾倒液体 | B. |  稀释浓硫酸 | C. |  灯帽盖灭酒精灯 | D. |  加热液体 |