题目内容
设四种未知元素为A,B,C,D.A-离子核外有18个电子;B原子最外层电子数比D原子核外电子数多2个,B原子比D原子多2个电子层;C元素的原子核外电子比B元素原子的核外电子多5个;D+离子的核外没有电子.
(1)写出这四种元素的名称及元素符号.
(2)画出各原子及A-离子的结构示意图.
(3)哪种元素非金属性最强?为什么?
(4)C元素有何化学特征?试用原子结构观点解释.
(1)写出这四种元素的名称及元素符号.
(2)画出各原子及A-离子的结构示意图.
(3)哪种元素非金属性最强?为什么?
(4)C元素有何化学特征?试用原子结构观点解释.
考点:物质的鉴别、推断,原子结构示意图与离子结构示意图,元素的符号及其意义
专题:元素推断题
分析:根据A- 离子核外有18个电子,说明A原子的核外电子数是17,依据核外电子数等于原子序数可知,所以A为氯元素;D+离子的核外没有电子,说明D原子的核外电子数是1个,所以D是氢元素;B原子比D原子多2个电子层,B原子最外层电子数比D原子核外电子数多2个,说明B原子的核外有3个电子层,且最外层的电子数是3,所以B原子最外层有13个电子,因此B是质子数为13的铝元素;C元素原子核外电子数比B原子多5个,说明C原子核外有18个电子,因此C是质子数为18的氩元素,然后结合题中的问题进行分析.
解答:解:(1)A- 离子核外有18个电子,说明A原子的核外电子数是17,依据核外电子数等于原子序数可知,所以A为氯元素,D+离子的核外没有电子,说明D原子的核外电子数是1个,所以D是氢元素,B原子比D原子多2个电子层,B原子最外层电子数比D原子核外电子数多2个,说明B原子的核外有3个电子层,且最外层的电子数是3,所以B原子最外层有13个电子,因此B是质子数为13的铝元素,C元素原子核外电子数比B原子多5个,说明C原子核外有18个电子,因此C是质子数为18的氩元素,所以A是氯元素,B是铝元素,C是氩元素,D是氢元素;故答案为:氯元素 Cl,铝元素 Al,氩元素 Ar,氢元素 H;
(2)氯原子的结构示意图: ;铝原子的结构示意图为:
;铝原子的结构示意图为: ;氩原子的结构示意图为:
;氩原子的结构示意图为: ;氢原子的结构示意图:
;氢原子的结构示意图: ,氯的离子的结构示意图
,氯的离子的结构示意图 ;故答案为:
;故答案为: ;
; ;
; ;
; ;
; ;
;
(3)同一周期从左到右非金属性增强,同一主族从上到下非金属性减弱,因此氢的非金属性最强;故答案为:氢;氢位于第一周期,同一周期从左到右非金属性增强,同一主族从上到下非金属性减弱;
(4)C元素是Ar,化学性质稳定,因为氩原子的最外层的电子数达到稳定结构;故答案为:化学性质稳定,因为氩原子的最外层的电子数达到稳定结构.
(2)氯原子的结构示意图:
 ;铝原子的结构示意图为:
;铝原子的结构示意图为: ;氩原子的结构示意图为:
;氩原子的结构示意图为: ;氢原子的结构示意图:
;氢原子的结构示意图: ,氯的离子的结构示意图
,氯的离子的结构示意图 ;故答案为:
;故答案为: ;
; ;
; ;
; ;
; ;
;(3)同一周期从左到右非金属性增强,同一主族从上到下非金属性减弱,因此氢的非金属性最强;故答案为:氢;氢位于第一周期,同一周期从左到右非金属性增强,同一主族从上到下非金属性减弱;
(4)C元素是Ar,化学性质稳定,因为氩原子的最外层的电子数达到稳定结构;故答案为:化学性质稳定,因为氩原子的最外层的电子数达到稳定结构.
点评:本题考查学生根据核外电子层排布情况及电子数之间的关系进行元素的推断,解题的能力.

练习册系列答案
相关题目
光亮的铁钉在下列几种情况下,最不容易生锈的是( )
A、 |
B、 |
C、 |
D、 |
以下是一些同学在这次化学实验操作考试中的做法,你认为正确的是( )
| A、把胶头滴管伸入试管中滴加液体 |
| B、在托盘天平上直接称量固体物质 |
| C、用药匙或纸槽把粉末药品送入试管底部 |
| D、握住试管夹的短柄给试管内的药品加热 |
下列图象与所述实验相符的是( )
A、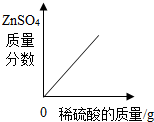 向一定量锌粒中加入过量稀硫酸 向一定量锌粒中加入过量稀硫酸 |
B、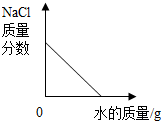 向一定量氯化钠饱和溶液中不断加入水 向一定量氯化钠饱和溶液中不断加入水 |
C、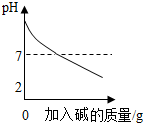 向pH=11的溶液中加入碱性溶液 向pH=11的溶液中加入碱性溶液 |
D、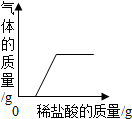 向一定量氢氧化钠和碳酸钠的混合溶液中加入稀盐酸 向一定量氢氧化钠和碳酸钠的混合溶液中加入稀盐酸 |
下列关于物质的组成及结构的说法中,正确的是( )
| A、汞是由银元素和水元素组成的 |
| B、水是由氧元素和氢分子组成的 |
| C、二氧化氮是由二氧化氮的分子构成的 |
| D、铁是由铁原子构成的 |
 实验装置如图所示.在干燥的圆底烧瓶里装满氯化氢气体,用带有玻璃管和预先吸水的胶头滴管的塞子塞紧瓶口,立即倒置烧瓶,使下端玻璃管插入烧杯内溶液中,打开止水夹,同时压缩滴管的胶头,使滴管少量水进入烧瓶,此时会看到的现象是:
实验装置如图所示.在干燥的圆底烧瓶里装满氯化氢气体,用带有玻璃管和预先吸水的胶头滴管的塞子塞紧瓶口,立即倒置烧瓶,使下端玻璃管插入烧杯内溶液中,打开止水夹,同时压缩滴管的胶头,使滴管少量水进入烧瓶,此时会看到的现象是: