题目内容
下列图象与所述实验相符的是( )
A、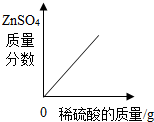 向一定量锌粒中加入过量稀硫酸 向一定量锌粒中加入过量稀硫酸 |
B、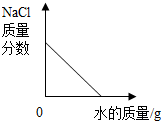 向一定量氯化钠饱和溶液中不断加入水 向一定量氯化钠饱和溶液中不断加入水 |
C、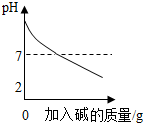 向pH=11的溶液中加入碱性溶液 向pH=11的溶液中加入碱性溶液 |
D、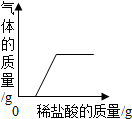 向一定量氢氧化钠和碳酸钠的混合溶液中加入稀盐酸 向一定量氢氧化钠和碳酸钠的混合溶液中加入稀盐酸 |
考点:金属的化学性质,溶质的质量分数,酸的化学性质,酸碱溶液的稀释
专题:元素化合物知识型
分析:A、根据锌与硫酸反应的过程分析;
B、根据溶液中溶质质量分数的计算公式分析;
C、根据碱性溶液和碱性溶液混合仍然为碱性溶液分析;
D、根据氢氧化钠与碳酸钠混合溶液中加盐酸,盐酸先与氢氧化钠反应,然后与碳酸钠反应分析.
B、根据溶液中溶质质量分数的计算公式分析;
C、根据碱性溶液和碱性溶液混合仍然为碱性溶液分析;
D、根据氢氧化钠与碳酸钠混合溶液中加盐酸,盐酸先与氢氧化钠反应,然后与碳酸钠反应分析.
解答:解:A、一定量的锌粒中加稀硫酸,硫酸锌的质量会不断变大直至锌完全反应,硫酸再过量硫酸锌的质量不会再增大,故此选项错误;
B、氯化钠饱和溶液中加入水,氯化钠的质量分数不断减小,但不会减小到0,故此选项错误;
C、向pH=11的溶液中加入碱性溶液,溶液应该仍然显碱性,因此pH应大于7,故此选项错误;
D、氢氧化钠与盐酸反应无现象,当氢氧化钠反应完全后,碳酸钠与盐酸反应产生气体,气体的量增大,当碳酸钠反应完后气体质量不再增加,故D正确;
故选D.
B、氯化钠饱和溶液中加入水,氯化钠的质量分数不断减小,但不会减小到0,故此选项错误;
C、向pH=11的溶液中加入碱性溶液,溶液应该仍然显碱性,因此pH应大于7,故此选项错误;
D、氢氧化钠与盐酸反应无现象,当氢氧化钠反应完全后,碳酸钠与盐酸反应产生气体,气体的量增大,当碳酸钠反应完后气体质量不再增加,故D正确;
故选D.
点评:此题是一道反应与图象的结合题,解题的关键是能结合反应分析各种量的变化关系,利用反应与图象相结合进行分析探讨,进而作出正确的判断.

练习册系列答案
 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
实验证明点燃的镁条在二氧化碳气体中可以燃烧,生成氧化镁和炭黑(碳单质).下列说法中错误的是( )
A、镁在二氧化碳中燃烧的化学方程式是:2Mg+CO2
| ||||
| B、镁条在空气中燃烧时只与二氧化碳发生了化学反应 | ||||
| C、金属镁着火不能用二氧化碳灭火器灭火 | ||||
| D、在上述反应中镁发生了氧化反应 |
含有杂质的硝酸铵样品,经测定其含氮元素的质量分数为38%,则其所含有的杂质一定有( )
| A、CO(NH2)2 |
| B、NH4HCO3 |
| C、NH4Cl |
| D、(NH4)2SO4 |
在相同的温度和压强下,相同体积的气体具有相同的分子数,反之亦然.取同温同压下相同体积的CO和O2混合,在一定条件下充分反应,恢复到初始温度和压强.下列说法正确的是( )
| A、参加反应的CO和O2的体积比为2:1 | ||
B、生成的CO2分子个数为原来气体分子数的
| ||
C、反应后气体的体积为原来的
| ||
| D、反应后的气体中C、O原子的个数比为1:2 |
2N表示( )
| A、两个氮元素 | B、两个氮原子 |
| C、两个氮分子 | D、氮气 |