题目内容
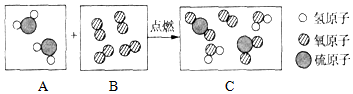
8.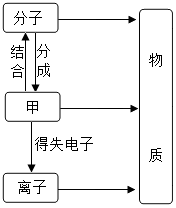 初中化学学习中,我们初步认识了物质的微观结构.构成物质的粒子之间的关系如图所示:
初中化学学习中,我们初步认识了物质的微观结构.构成物质的粒子之间的关系如图所示:(1)甲是原子.…
(2)在水,水银,硫酸铜三种物质中,由离子构成的物质是氯化钠,它由钠离子和氯离子组成.
(3)用化学用语填空:2个钙离子2Ca2+; 70个碳原子构成的一种新分子C70; 保持氢气化学性质的最小粒子是H2,水分子H2O
(4)写出数字“2”意义:CO32-中“2”的意义:一个碳酸根离子带有2个单位的负电荷.
(5)元素周期表中某一周期元素的原子结构示意图如下:
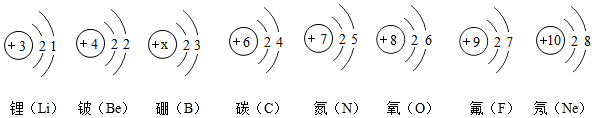
①图中这些元素都处于第2周期.硼原子结构示意图中的X=5.
②镁原子的结构示意图为
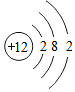 ,上图中与其化学性质相似的元素是Be.
,上图中与其化学性质相似的元素是Be.这两种原子在化学反应中容易失去电子(填“得到”或“失去”).
③图中元素从左到右排列所遵循的规律是(任写一条)核电荷数依次递增.
④根据图示信息确定1个一氧化碳分子中所含电子总数为14.
分析 根据物质的微观构成粒子、符号的书写以及化学符号周围数字的意义进行分析解答,在原子中,核內质子数等于核外电子数,元素的化学性质与原子的最外层电子数有关,据此解答.
解答 解:(1)甲是能构成分子,能形成离子,故甲是原子,故填:原子.
(2)在水,水银,硫酸铜三种物质中,氯化钠是由离子构成的物质,它由钠离子和氯离子组成,故填:氯化钠;钠离子和氯离子.
(3)2个钙离子就是在钙离子的前面加上数字2,故填:2Ca2+;
70个碳原子构成的一种新分子,就是在碳元素符号的右下角加上数字70,故填:C70;
保持氢气化学性质的最小粒子是氢分子,故填:H2;
水分子的符号为:H2O,故填:H2O;
(4)CO32-中“2”表示一个碳酸根离子带有2个单位的负电荷,故填:一个碳酸根离子带有2个单位的负电荷.
(5)①图中这些元素的原子核外有2个电子层,故都处于第2周期.在原子中核內质子数-核外电子数,故硼原子结构示意图中的X=2+3=5,故填:2;5.
②元素的化学性质与原子的最外层电子数有关,镁原子的结构示意图中最外层有2个电子,故图中与其化学性质相似的元素是Be,故填:Be.
这两种原子在化学反应中容易失去电子,故填:失去.
③图中元素从左到右排列所遵循的一条规律是核电荷数依次递增,故填:核电荷数依次递增.
④1个一氧化碳分子中所含电子总数为:6+8=14,故填:14.
点评 本题考查的是物质的微观构成粒子的知识,完成此题,可以依据已有的知识结合题干提供的信息进行.

练习册系列答案
相关题目
3.下列实验操作符合规范的是( )
| A. |  | B. |  | C. |  | D. |  |
20.硫酸铜是一种应用极其广泛的化工原料,易溶于水而不易溶于酒精;铜离子完全沉淀的pH是5左右,铁离子完全沉淀的pH是2左右.以下是某工厂用含铁废铜为原料生产胆矾(CuSO4•5H2O)和副产物石膏(CaSO4•2H2O)的生产流程示意图:
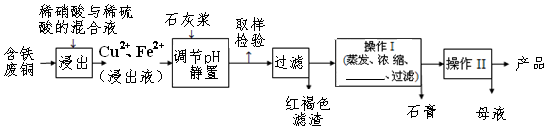
胆矾和石膏在不同温度下的溶解度(g/100g水)如表.
请回答下列问题:
(1)红褐色滤渣的主要成分是Fe(OH)3;
(2)石灰浆调pH大约要调节到A
A.2 B.5 C.7 D.10
(3)含铁的废铜和稀硫酸反应的化学方程式Fe+H2SO4=FeSO4+H2↑;
(4)操作I最后温度应该控制在100℃左右;
(5)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、降温结晶、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是硫酸铜是易溶于水而不易溶于酒精.

胆矾和石膏在不同温度下的溶解度(g/100g水)如表.
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
(1)红褐色滤渣的主要成分是Fe(OH)3;
(2)石灰浆调pH大约要调节到A
A.2 B.5 C.7 D.10
(3)含铁的废铜和稀硫酸反应的化学方程式Fe+H2SO4=FeSO4+H2↑;
(4)操作I最后温度应该控制在100℃左右;
(5)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、降温结晶、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是硫酸铜是易溶于水而不易溶于酒精.