题目内容
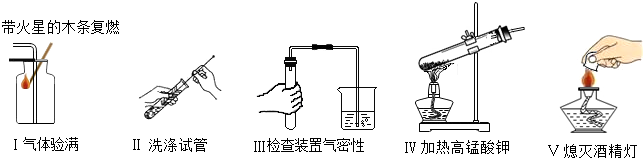
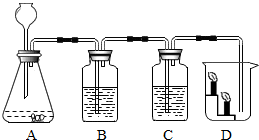
 为了证明铁、银、铜三种金属的活动性顺序小明同学利用如图所示装置进行了探究.请回答下列问题.
为了证明铁、银、铜三种金属的活动性顺序小明同学利用如图所示装置进行了探究.请回答下列问题.(1)请写出装置中两种金属片和溶液中的溶质应分别选择什么物质 (写出一组即可).
(2)上述探究实验的结论是什么?并写出得出结论所依据的实验现象是什么.
(3)请写出上述探究实验中发生反应的化学方程式.
考点:金属活动性顺序及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答:解:铁排在氢前面,铜和银都排在氢后面,因此利用金属与酸反应时,铜和银与酸都不反应,所以不能用金属与酸反应;利用如图所示装置进行探究,可以利用金属与盐溶液的反应,可以将铁和银分别放入硫酸铜溶液中,铁能置换出铜,铁片表面有红色物质覆盖,而银不能置换出铜,银片表面无明显现象;由此可得出结论说:三种金属的活动性顺序为:Fe>Cu>Ag,
化学方程为:Fe+CuSO4=Cu+FeSO4
故答案为:
(1)装置中两种金属片和溶液中的溶质应分别选择Fe、Ag、CuS04溶液(其他合理答案也可);
(2)上述探究实验的结论是:三种金属的活动性顺序为:Fe>Cu>Ag;得出结论所依据的实验现象是:铁片表面有红色物质覆盖,而银片表面无明显现象;
(3)上述探究实验中发生反应的化学方程式:Fe+CuS04═FeS04+Cu
化学方程为:Fe+CuSO4=Cu+FeSO4
故答案为:
(1)装置中两种金属片和溶液中的溶质应分别选择Fe、Ag、CuS04溶液(其他合理答案也可);
(2)上述探究实验的结论是:三种金属的活动性顺序为:Fe>Cu>Ag;得出结论所依据的实验现象是:铁片表面有红色物质覆盖,而银片表面无明显现象;
(3)上述探究实验中发生反应的化学方程式:Fe+CuS04═FeS04+Cu
点评:同学们要会利用金属活动顺序表设计实验,去验证金属的活动性强弱.氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目