题目内容
8.向含有AgNO3、Cu(NO3)2的混合溶液中,加入一定量铁粉,充分反应后过滤,往滤渣中加入稀硫酸,有气泡产生,则滤液中大量存在的离子是( )| A. | Fe2+、NO3- | B. | Fe2+、H+、NO3- | ||
| C. | Fe2+、Cu2+、NO3- | D. | Fe2+、Cu2+、Ag+、NO3- |
分析 在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.据此分析判断有关的问题.
解答 解:由于金属的活动性顺序是:铁>铜>银,向含有AgNO3、Cu(NO3)2的混合溶液中,加入一定量铁粉,铁先与硝酸银反应生成了硝酸亚铁和银,当硝酸银完全反应后,铁再与硝酸铜反应生成了硝酸亚铁和铜.由充分反应后过滤,往滤渣中加入稀硫酸,有气泡产生,说明了铁有剩余,溶液中的银和铜完全被置换出来了.则溶液中只含有硝酸亚铁.由此可知,A正确,BCD错误.
故选A.
点评 本题是对金属活动性顺序的考查,解题的关键是掌握金属活动性顺序表的意义,只有这样才能做出正确的判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列关于空气飞说法不正确的是( )
| A. | 主要成分是氮气和氧气 | |
| B. | 各种成分的含量相对稳定 | |
| C. | 是一种十分重要的天然资源 | |
| D. | 空气污染指数越高说明空气质量越好 |
19.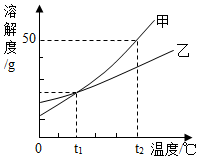 图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
 图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | 甲中含有少量的乙,可以用蒸发溶剂的方法提纯乙 | |
| C. | t2℃时,将等质量的甲、乙两种物质的溶液分别降温至t1℃,析出晶体的质量甲一定大于乙 | |
| D. | t2℃时,乙饱和溶液中溶质的质量分数一定小于甲饱和溶液中溶质的质量分数 |
3.空气中能用作粮食保护气同时可制氮肥的是( )
| A. | 氧气 | B. | 二氧化碳 | C. | 水蒸气 | D. | 氮气 |
15.下列说法中,正确的是( )
| A. | S、P都属于易燃物,与氧气接触都能立刻燃烧 | |
| B. | C、CO高温条件下都能还原Fe2O3,都具有氧化性 | |
| C. | NaOH、Ca(OH)2都是常见的碱,都可用于改良酸性土壤 | |
| D. | NH4Cl、NH4NO3都含有NH4+离子,与熟石灰混合后研磨都能生成有氨味的气体 |
