题目内容
5.下面是石建和俞悦同学在实验技能竞赛中抽到的一道试题,三瓶失去标签的溶液,分别是酸(初中常见的酸)、氢氧化钡溶液和碳酸钾溶液.作为他们的参赛伙伴,请你和他们共同完成以下探究:【提出问题】三种溶液中的溶质分别是什么?
【制定计划】通过比较这三类物质的化学性质,俞悦同学认为不需要再选择试剂,只要通过三种物质间相互反应产生的现象,便可确定三种溶液中的溶质.
【探究实验1】

【表达与交流】根据实验现象,石建同学认为3号溶液一定是氢氧化钡溶液,酸一定是 稀硫酸.你认为他的结论正确(填“正确”或“不正确”).
【探究实验2】取探究实验1乙试管中的固液混合物继续进行如下实验:

【反思与评价】经过和小组同学的深入探讨,俞悦认为无法根据此现象确定1号和2号溶液成分,请你对俞悦同学的结论给予评价正确,因为如果1号是稀硫酸,则少量的稀硫酸和乙中的碳酸钡反应生成的二氧化碳能够被氢氧化钾吸收,无气泡产生,并且稀硫酸和碳酸钡反应生成硫酸钡沉淀,因此白色沉淀无明显变化;如果1号是碳酸钾,则碳酸钾和氢氧化钾、硫酸钡不能反应,无气泡产生,白色沉淀无明显变化,因此无法根据此现象确定1号和2号溶液成分.
【解释与结论】取探究实验2丙试管中的固液混合物继续如下实验:

用化学方程式表示丁试管中产生气泡且白色沉淀不减少的原因BaCO3+H2SO4═BaSO4↓+H2O+CO2↑(写出一定能发生的反应即可).经过共同努力,小组同学最终确定了三种溶液中分别含有的溶质的成分,请将三种溶液溶质的化学式分别标在试剂瓶的标签中.
分析 【表达与交流】
氢氧化钡能和稀硫酸反应生成白色沉淀硫酸钡和水,能和碳酸钾反应生成白色沉淀碳酸钡和氢氧化钾;
【反思与评价】
稀硫酸和碳酸钡反应生成白色沉淀硫酸钡、水和二氧化碳;
碳酸钾和硫酸钡不能反应;
【解释与结论】
根据实验现象、反应物和生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.
解答 解:【表达与交流】
因为氢氧化钡能和稀硫酸反应生成硫酸钡沉淀和水,能和碳酸钾反应生成碳酸钡沉淀和氢氧化钾,因此3号溶液一定是氢氧化钡溶液,酸一定是稀硫酸,所以他的结论是正确的.
故填:正确.
【反思与评价】
因为如果1号是稀硫酸,则少量的稀硫酸和乙中的碳酸钡反应生成的二氧化碳能够被氢氧化钾吸收,无气泡产生,并且稀硫酸和碳酸钡反应生成硫酸钡沉淀,因此白色沉淀无明显变化;如果1号是碳酸钾,则碳酸钾和氢氧化钾、硫酸钡不能反应,无气泡产生,白色沉淀无明显变化,因此无法根据此现象确定1号和2号溶液成分,因此俞悦同学的结论是正确的.
故填:正确,因为如果1号是稀硫酸,则少量的稀硫酸和乙中的碳酸钡反应生成的二氧化碳能够被氢氧化钾吸收,无气泡产生,并且稀硫酸和碳酸钡反应生成硫酸钡沉淀,因此白色沉淀无明显变化;如果1号是碳酸钾,则碳酸钾和氢氧化钾、硫酸钡不能反应,无气泡产生,白色沉淀无明显变化,因此无法根据此现象确定1号和2号溶液成分.
【解释与结论】
因为稀硫酸能和碳酸钡反应生成硫酸钡沉淀、水和二氧化碳,因此1号溶液是稀硫酸,2号溶液是碳酸钾溶液,3号溶液是氢氧化钡溶液,碳酸钡和稀硫酸反应的化学方程式为:
BaCO3+H2SO4═BaSO4↓+H2O+CO2↑.
故填:BaCO3+H2SO4═BaSO4↓+H2O+CO2↑.
三种溶液溶质的化学式标在试剂瓶的标签中,如下图所示:
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A. | 由碳原子、氢原子、氧原子构成 | |
| B. | 酚酞中碳、氢、氧三种原子的个数比是10:7:2 | |
| C. | 相对分子质量为318g | |
| D. | 酚酞分子中所含碳元素的质量分数最大 |
| A. | 化学与健康 ①食用鲜黄瓜-可大量补钙 ②人体缺铁-易患贫血病 | |
| B. | 化学与生活 ①减轻车内异味-开窗通风 ②防止食品受潮-用氧化钙做干燥剂 | |
| C. | 化学与安全 ①重金属盐中毒-喝鲜牛奶解毒 ②煤气泄漏-关闭阀门,严禁烟火 | |
| D. | 化学与环境 ①使用乙醇汽油-减少空气污染 ②合理使用农药、化肥-减少水污染 |
| A. | 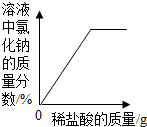 向一定的NaOH溶液中滴加稀HCl | |
| B. | 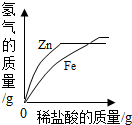 向相同质量的铁粉和锌粉中分别加入足量稀盐酸 | |
| C. | 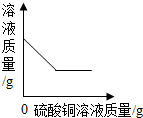 向一定量的铁粉中不断加入硫酸铜溶液 | |
| D. | 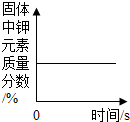 加热一定质量的高锰酸钾 |
| A. | 维生素C是由6个碳原子、8个氢原子和6个氧原子构成的 | |
| B. | 维生素C由碳、氢、氧三种元素组成的 | |
| C. | 维生素C的相对分子质量是168 | |
| D. | 维生素C中碳、氢、氧元素的质量比为3:4:3 |
| A. | 硫在氧气中燃烧产生明亮的蓝紫色火焰 | |
| B. | 经回火处理后的钢针可以用来制作鱼钩 | |
| C. | 洗洁精具有乳化作用,能去除餐具上的油污 | |
| D. | 合金的硬度比组成它们的纯金属的硬度小 |
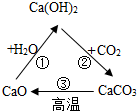 完成下列反应的化学方程式,并回答有关问题,请你用化学方程式表示如图中的三个化学反应
完成下列反应的化学方程式,并回答有关问题,请你用化学方程式表示如图中的三个化学反应 A、B、C、D、E为五种不同类别的纯净物,他们之间的反应关系如图.“”表示两种物质之间能相互转化,“-”表示两物质之间能发生化学反应.其中,A为金属单质,B为赤铁矿的主要成分,E的水溶液为黄色.请回答:
A、B、C、D、E为五种不同类别的纯净物,他们之间的反应关系如图.“”表示两种物质之间能相互转化,“-”表示两物质之间能发生化学反应.其中,A为金属单质,B为赤铁矿的主要成分,E的水溶液为黄色.请回答: