题目内容
19.某合金由两种金属元素组成,取该合金60g投入足量稀硫酸中,反应完全后,测得生成H2 2g,则合金的组成不可能是( )| A. | Fe与Zn | B. | Mg与Cu | C. | Zn与Al | D. | Al与Fe |
分析 首先判断金属能否与酸反应,然后从金属与酸反应生成氢气的质量关系考虑.根据化学方程式,可得出如下金属与氢气的质量关系:Mg-H2:24-2 Al-H2:18-2 Fe-H2:56-2 Zn-H2:65-2;利用平均值法来判断即可得出正确的答案.
解答 解:根据化学方程式已知金属与氢气的质量关系:Mg-H2:24g-2g;同理可知:Al-H2:18g-2g; Fe-H2:56g-2g;Zn-H2:65g-2g;利用平均值法得知要生成2克氢气,合金的质量应该符合:金属A的数值<60g<金属B的数值.
A、56g和65g均大于60g,所以合金的组成可能,故A正确;
B、24g小于60g,Cu不与酸反应,不产生氢气,所以合金的组成可能,故B正确;
C、18g<60g<65g,所以合金的组成可能,故C正确;
D、18g、56g都小于60,所以合金的组成不可能,故D错误.
故选:D.
点评 此题要利用平均值法来解决,从金属与酸反应生成氢气的质量关系考虑得出金属与氢气的质量关系,对解决此类题目很有帮助.

练习册系列答案
相关题目
7.t2℃时,将甲、乙固体各W g (不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,降温到t1℃时现象如图2(水分不蒸发),甲、乙固体的溶解度曲线如图3.

下列说法正确的是( )

下列说法正确的是( )
| A. | 图3中M表示的是乙的溶解度曲线 | |
| B. | 图2中甲溶液一定饱和,乙溶液一定饱和 | |
| C. | 图2乙溶液一定比甲溶液浓 | |
| D. | 当W=50g时,甲、乙溶液溶质质量分数一定相等 |
3.实验小组同学通过以下实验研究二氧化碳的性质.
(1)该实验可以说明分子具有的性质是分子是不断运动的.
(2)烧杯内壁上贴干的紫色石蕊纸条的目的是证明干燥的二氧化碳不能使紫色的石蕊试液变红色.
(3)该实验得出的结论是二氧化碳与水反应生成了碳酸.
(4)写出二氧化碳遇到石灰水发生反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
| 实验装置 | 实验操作 | 实验现象 |
 | ①在烧杯内壁上贴上干的和用水润湿的紫色石蕊纸条 ②将充满二氧化碳的敞口集气瓶轻轻放入烧杯中 | 一段时间后,湿的紫色石蕊纸条变为红色 |
(2)烧杯内壁上贴干的紫色石蕊纸条的目的是证明干燥的二氧化碳不能使紫色的石蕊试液变红色.
(3)该实验得出的结论是二氧化碳与水反应生成了碳酸.
(4)写出二氧化碳遇到石灰水发生反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
10.化学对环境的保护和改善起着重要作用,下列做法错误的是( )
| A. | 工业废水经处理达标后再排放 | |
| B. | 化石燃料燃烧会造成空气污染,应禁止使用 | |
| C. | 改进燃煤炉灶,促进燃料充分燃烧 | |
| D. | 使用汽油和柴油的汽车尾气应采用催化净化装置,将有害气体转化为无害物质 |
7.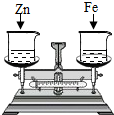 如图所示,天平调平后,在天平两盘的烧杯中各加入质量相等、质量分数相等足量的稀盐酸,同时向其中分别加入少量质量相等的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是( )
如图所示,天平调平后,在天平两盘的烧杯中各加入质量相等、质量分数相等足量的稀盐酸,同时向其中分别加入少量质量相等的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是( )
 如图所示,天平调平后,在天平两盘的烧杯中各加入质量相等、质量分数相等足量的稀盐酸,同时向其中分别加入少量质量相等的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是( )
如图所示,天平调平后,在天平两盘的烧杯中各加入质量相等、质量分数相等足量的稀盐酸,同时向其中分别加入少量质量相等的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是( )| A. | 向左偏 | B. | 向右偏 | ||
| C. | 先向左偏后向右偏 | D. | 先向右偏后向左偏 |
8.葡萄糖是生活中常见的物质,某兴趣小组对“葡萄糖的组成”进行了探究.
【查阅资料】绿色植物通过光合作用将二氧化碳和水转化成葡萄糖和氧气.
【实验探究】
方案一:小明将葡萄糖在氧气中燃烧,检验到生成物中有水和二氧化碳,得出结论“葡萄糖是由碳、氢、氧三种元素组成的”.
小刚认为该方案不合理,实验只能说明葡萄糖中一定含有由于元素种类在化学反应前后都不发生变化,生成物中有二氧化碳和水生成,说明反应物中也应该含有碳、氢、氧元素,而氧气中含有氧元素,因此该物质中一定含有碳、氢元素,可能含有氧元素元素,
方案二:小刚用如图所示装置进行实验,实验开始先通入一会儿氮气,然后关闭弹簧夹,点燃酒精灯给葡萄糖加强热.

(1)先通氮气的原因是排净装置中的空气,避免对实验造成干扰,观察到小烧杯中有水雾出现出现,说明葡萄糖中含有氢、氧元素.
(2)观察到硬质玻璃管中残留有黑色固体,他猜测该黑色固体是单质碳,并继续利用如图装置,另选试剂进行了验证单质碳的实验.实验过程和现象如表:
实验现象②对应的文字(或符号)表达式:CO2+Ca(OH)2═CaCO3↓+H2O.
【实验结论】葡萄糖是由碳、氢、氧三种元素组成的.
【查阅资料】绿色植物通过光合作用将二氧化碳和水转化成葡萄糖和氧气.
【实验探究】
方案一:小明将葡萄糖在氧气中燃烧,检验到生成物中有水和二氧化碳,得出结论“葡萄糖是由碳、氢、氧三种元素组成的”.
小刚认为该方案不合理,实验只能说明葡萄糖中一定含有由于元素种类在化学反应前后都不发生变化,生成物中有二氧化碳和水生成,说明反应物中也应该含有碳、氢、氧元素,而氧气中含有氧元素,因此该物质中一定含有碳、氢元素,可能含有氧元素元素,
方案二:小刚用如图所示装置进行实验,实验开始先通入一会儿氮气,然后关闭弹簧夹,点燃酒精灯给葡萄糖加强热.

(1)先通氮气的原因是排净装置中的空气,避免对实验造成干扰,观察到小烧杯中有水雾出现出现,说明葡萄糖中含有氢、氧元素.
(2)观察到硬质玻璃管中残留有黑色固体,他猜测该黑色固体是单质碳,并继续利用如图装置,另选试剂进行了验证单质碳的实验.实验过程和现象如表:
| 实验过程 | 实验现象 |
小烧杯中放入澄清的石灰水,往硬质玻璃管中通入氧气,点燃酒精,进行加热 | ①硬质玻璃管中的黑色固体剧烈燃烧,发出白光; ②澄清的石灰水变浑浊 |
【实验结论】葡萄糖是由碳、氢、氧三种元素组成的.

