题目内容
小张同学得知我国早在西汉时期,就能利用铁单质与硫酸铜溶液反应制取铜,其反应的化学方程式为 .他利用硫酸铜进行趣味实验,将浸泡了 色硫酸铜溶液的滤纸在酒精灯火焰上点燃,观察到滤纸颜色变白,由湿变干后燃烧.在燃烧后的灰烬中出现红色固体.他很好奇,进行了相关探究,请你参与并填写有关空白.
【提出问题】
红色固体是什么物质?它是如何产生的?
【查阅资料】
(1)温度达200℃时,CuSO4开始分解生成CuO和另一种氧化物;此反应前后各元素的化合价保持不变.
(2)温度超过1000℃,CuO才分解生成氧化亚铜(Cu2O);Cu2O呈红色.
【作出猜想】红色固体①可能是Cu;②也可能是Cu2O;③还可能是 的混合物.
【实验探究】
(1)取红色固体观赏,呈亮红色;
(2)取少量红色固体于试管中,加入稀硫酸,固体不溶解,溶液仍为无色.
【分析推理】
(1)请教老师后得知,如有Cu2O存在,加入稀硫酸会发生如下反应:Cu2O+H2SO4═CuSO4+Cu+H2O结合实验探究的现象,确定亮红色固体为 ,同时也说明滤纸燃烧时的温度低于 (填序号)
A.200℃B.1000℃
(2)滤纸主要是由碳、氢、氧三种元素组成的,经分析,产生红色固体的原因可能是滤纸在燃烧过程中产生的碳与分解产生的CuO发生反应,生成亮红色固体和二氧化碳,请写出该反应的化学方程式 .
【交流讨论】
(1)将浸有硫酸铜溶液的滤纸点燃,刚开始不能燃烧,是因为 .
(2)此实验中,CuSO4受热分解生成CuO和 (填化学式).
【提出问题】
红色固体是什么物质?它是如何产生的?
【查阅资料】
(1)温度达200℃时,CuSO4开始分解生成CuO和另一种氧化物;此反应前后各元素的化合价保持不变.
(2)温度超过1000℃,CuO才分解生成氧化亚铜(Cu2O);Cu2O呈红色.
【作出猜想】红色固体①可能是Cu;②也可能是Cu2O;③还可能是
【实验探究】
(1)取红色固体观赏,呈亮红色;
(2)取少量红色固体于试管中,加入稀硫酸,固体不溶解,溶液仍为无色.
【分析推理】
(1)请教老师后得知,如有Cu2O存在,加入稀硫酸会发生如下反应:Cu2O+H2SO4═CuSO4+Cu+H2O结合实验探究的现象,确定亮红色固体为
A.200℃B.1000℃
(2)滤纸主要是由碳、氢、氧三种元素组成的,经分析,产生红色固体的原因可能是滤纸在燃烧过程中产生的碳与分解产生的CuO发生反应,生成亮红色固体和二氧化碳,请写出该反应的化学方程式
【交流讨论】
(1)将浸有硫酸铜溶液的滤纸点燃,刚开始不能燃烧,是因为
(2)此实验中,CuSO4受热分解生成CuO和
考点:实验探究物质的性质或变化规律,酸的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:根据铁单质与硫酸铜溶液反应制取铜,写出反应的化学方程式,根据铜离子显蓝色解答;
【作出猜想】根据温度超过1000℃,CuO才分解生成氧化亚铜(Cu2O);Cu2O呈红色,则CuO的生成物可能为Cu,也可能为Cu2O,还有可能为Cu、Cu2O的混合物;
【分析推理】
(1)根据所设计的实验:向红色固体中加入足量稀硫酸,由于铜不能与稀硫酸发生反应而Cu2O能与稀硫酸反应生成铜和硫酸铜,反应后溶液呈蓝色说明固体中含有Cu2O;若无现象,则固体中只含有铜;
(2)根据碳与CuO发生反应,生成亮红色固体和二氧化碳,写出反应的化学方程式;
【交流讨论】
(1)根据燃烧的条件解答;
(2)根据CuSO4开始分解生成CuO和另一种氧化物;此反应前后各元素的化合价保持不变,利用质量守恒定律解答.
【作出猜想】根据温度超过1000℃,CuO才分解生成氧化亚铜(Cu2O);Cu2O呈红色,则CuO的生成物可能为Cu,也可能为Cu2O,还有可能为Cu、Cu2O的混合物;
【分析推理】
(1)根据所设计的实验:向红色固体中加入足量稀硫酸,由于铜不能与稀硫酸发生反应而Cu2O能与稀硫酸反应生成铜和硫酸铜,反应后溶液呈蓝色说明固体中含有Cu2O;若无现象,则固体中只含有铜;
(2)根据碳与CuO发生反应,生成亮红色固体和二氧化碳,写出反应的化学方程式;
【交流讨论】
(1)根据燃烧的条件解答;
(2)根据CuSO4开始分解生成CuO和另一种氧化物;此反应前后各元素的化合价保持不变,利用质量守恒定律解答.
解答:解:
铁单质与硫酸铜溶液反应制取铜,反应的化学方程式为:CuSO4+Fe═Cu+FeSO4,铜离子显蓝色,硫酸铜溶液是蓝色溶液;
【作出猜想】根据温度超过1000℃,CuO才分解生成氧化亚铜(Cu2O);Cu2O呈红色,铜也是红色,;③还可能是Cu、Cu2O的混合物;
【分析推理】
(1)由于铜不能与稀硫酸发生反应而Cu2O能与稀硫酸反应生成铜和硫酸铜,反应后溶液呈蓝色说明固体中含有Cu2O;若无现象,则固体中只含有铜;根据探究,取少量红色固体于试管中,加入稀硫酸,固体不溶解,溶液仍为无色,则固体中只含有铜;同时也说明滤纸燃烧时的温度低于1000℃;
(2)碳与CuO发生反应,生成亮红色固体和二氧化碳,反应的化学方程式为:C+2CuO
2Cu+CO2↑;
【交流讨论】
(1)将浸有硫酸铜溶液的滤纸点燃,刚开始不能燃烧,是因为没有达到燃烧所需的最低温度(着火点);
(2)CuSO4开始分解生成CuO和另一种氧化物;此反应前后各元素的化合价保持不变,故CuSO4受热分解生成CuO和SO3.
故答案为:
CuSO4+Fe═Cu+FeSO4;蓝;
【作出猜想】③Cu、Cu2O;
【分析推理】
(1)铜;B;
(2)C+2CuO
2Cu+CO2↑;
【交流讨论】
(1)没有达到燃烧所需的最低温度(着火点);
(2)SO3.
铁单质与硫酸铜溶液反应制取铜,反应的化学方程式为:CuSO4+Fe═Cu+FeSO4,铜离子显蓝色,硫酸铜溶液是蓝色溶液;
【作出猜想】根据温度超过1000℃,CuO才分解生成氧化亚铜(Cu2O);Cu2O呈红色,铜也是红色,;③还可能是Cu、Cu2O的混合物;
【分析推理】
(1)由于铜不能与稀硫酸发生反应而Cu2O能与稀硫酸反应生成铜和硫酸铜,反应后溶液呈蓝色说明固体中含有Cu2O;若无现象,则固体中只含有铜;根据探究,取少量红色固体于试管中,加入稀硫酸,固体不溶解,溶液仍为无色,则固体中只含有铜;同时也说明滤纸燃烧时的温度低于1000℃;
(2)碳与CuO发生反应,生成亮红色固体和二氧化碳,反应的化学方程式为:C+2CuO
| ||
【交流讨论】
(1)将浸有硫酸铜溶液的滤纸点燃,刚开始不能燃烧,是因为没有达到燃烧所需的最低温度(着火点);
(2)CuSO4开始分解生成CuO和另一种氧化物;此反应前后各元素的化合价保持不变,故CuSO4受热分解生成CuO和SO3.
故答案为:
CuSO4+Fe═Cu+FeSO4;蓝;
【作出猜想】③Cu、Cu2O;
【分析推理】
(1)铜;B;
(2)C+2CuO
| ||
【交流讨论】
(1)没有达到燃烧所需的最低温度(着火点);
(2)SO3.
点评:在研究物质组成时,通过定性的探究实验不能确定某组成成分时,可通过定量研究加以判断;定量研究时,质量守恒思想是进行推断的根本依据.

练习册系列答案
相关题目
盐酸的下列用途中,能用硫酸代替盐酸的是( )
| A、实验室制取二氧化碳 |
| B、洗去盛放过石灰水瓶壁上的白膜 |
| C、金属表面除锈 |
| D、除去氯化钠中含有的少量氢氧化钠 |

 中和反应在工农业生产中应用广泛,现向40g 10%的氢氧化钠溶液中不断滴加盐酸,同时测定溶液pH的变化(曲线如图),请分析计算:
中和反应在工农业生产中应用广泛,现向40g 10%的氢氧化钠溶液中不断滴加盐酸,同时测定溶液pH的变化(曲线如图),请分析计算:
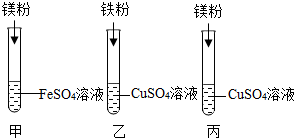 某化学兴趣小组同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的实验方案
某化学兴趣小组同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的实验方案