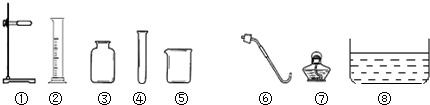
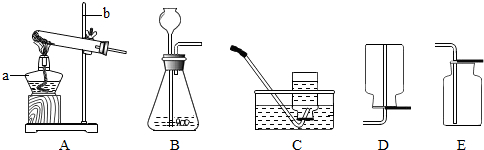
��Ŀ����
�������⣨H2O2������ɫҺ�壬��ˮ��Һ�׳�˫��ˮ����һ��Ư������������
��1��ijҽԺ��Ҫ3%��˫��ˮ30kg�����ú���������30%����Һ�����ƣ���Ҫ����Һ����ǧ�ˣ�
��2��ʵ���ҳ��ù��������ڶ������̴���ȡ��������Ҫ��ȡ8g����������������Ҫ���ٿ�������������Ϊ20%�Ĺ���������Һ��
����ѧ����ʽΪ2H2O2
2H2O+O2����
��1��ijҽԺ��Ҫ3%��˫��ˮ30kg�����ú���������30%����Һ�����ƣ���Ҫ����Һ����ǧ�ˣ�
��2��ʵ���ҳ��ù��������ڶ������̴���ȡ��������Ҫ��ȡ8g����������������Ҫ���ٿ�������������Ϊ20%�Ĺ���������Һ��
����ѧ����ʽΪ2H2O2
| ||
��������1������ϡ��ǰ�����ʵ���������������
��2�������������������ø÷�Ӧ�ķ���ʽ��ɣ�
��2�������������������ø÷�Ӧ�ķ���ʽ��ɣ�
����⣺��1������Ҫ30%����������Һ������Ϊx
x��30%=30Kg��3%
x=3Kg
��2������Ҫ20%�Ĺ���������Һ������Ϊy
2H2O2
2H2O+O2��
68�������������� 32
y��20% 8g
=
y=85g
�𣺣�1����Ҫ����Һ3Kg����2����������Ҫ85g��������Ϊ20%�Ĺ���������Һ��
x��30%=30Kg��3%
x=3Kg
��2������Ҫ20%�Ĺ���������Һ������Ϊy
2H2O2
| ||
68�������������� 32
y��20% 8g
| 68 |
| y��20% |
| 32 |
| 8g |
y=85g
�𣺣�1����Ҫ����Һ3Kg����2����������Ҫ85g��������Ϊ20%�Ĺ���������Һ��
�����������Ƕ���Һϡ���Լ���ѧ����ʽ����Ŀ����⣬���ͻ�����Ҫ����صĻ������㷽����

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
 ʵ�����г��ø���������ȷֽ���ȡ������
ʵ�����г��ø���������ȷֽ���ȡ������