题目内容
7.2月6日发生的台湾南部地震造成生命财产重大损失,造成116人罹难、500多人受伤,同时导致土壤液化、民宅倒塌、学校设施受损、民众心理受创等后遗症,亟需展开灾后重建.为防止灾后疫情出现,防疫人员用过氧乙酸(C2H4O3)、次氯酸钠(NaClO)进行消毒.下列说法正确的是( )| A. | 次氯酸钠中氯元素的化合价为-1 | |
| B. | 次氯酸钠是氧化物 | |
| C. | 过氧乙酸的相对分子质量为76 | |
| D. | 过氧乙酸中碳、氢、氧元素的质量比为2:4:3 |
分析 A、根据在化合物中正负化合价代数和为零,进行解答;
B、根据氧化物是指由两种元素组成且其中一种是氧元素的化合物,进行解分析解答;
C、根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行解答;
D、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答.
解答 解:A、根据在化合物中正负化合价代数和为零,可得次氯酸钠中氯元素的化合价为:(+1)+x+(-2)=0,则x=+1;故A错误;
B、根据氧化物是指由两种元素组成且其中一种是氧元素的化合物,次氯酸钠由三种元素组成,故B错误;
C、根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得过氧乙酸的相对分子质量为:12×2+1×4+16×3=76;故C正确;
D、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可知过氧乙酸中碳、氢、氧元素的质量比为:12×2:1×4:16×3=6:1:12,故D错误;
故选:C.
点评 本题考查学生对化合物中元素化合价,相对分子的质量,各元素质量比的计算能力及对氧化物的概念的理解与掌握

练习册系列答案
相关题目
17.铁、铝、铜是常见的三种金属.同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理.
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格.
将粗细相同的铁丝、铝丝、铜丝分别插人体积相同、溶质质量分数也相同的稀盐酸中:
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面致密的氧化膜会先与盐酸反应.
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是除去金属表面的氧化物.
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
写出铁与硫酸铜溶液反应的化学方程式Fe+CuSO4=FeSO4+Cu.
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插人顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序.金属丝的插入顺序为铜铁铝或铁铜铝.
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序Cu、Fe、Al.
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格.
将粗细相同的铁丝、铝丝、铜丝分别插人体积相同、溶质质量分数也相同的稀盐酸中:
| 操作 | 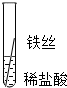 |  | 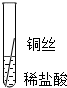 | 根据现象得出金属活动性顺序 |
| 片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al,Fe>Cu |
| 几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 |
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是除去金属表面的氧化物.
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
| 操作 |  | 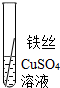 | 根据现象得出金属活动性顺序 |
| 现象 | 无明显现象 | 铁丝表面有红色物质析出 | Al>Fe>Cu |
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插人顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序.金属丝的插入顺序为铜铁铝或铁铜铝.
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序Cu、Fe、Al.
2.2015年,三沙市继续加大生态保护力度,加快海水淡化设施和太阳能等设备在有居民岛礁全覆盖,实现永兴岛不再提取地下水,下列有关海水淡化的方法在原理上完全不可行的是( )
| A. | 加明矾使海水中的盐分沉淀而淡化 | |
| B. | 利用太阳能加热 使之沸腾汽化,再把蒸汽冷凝成淡水的方法 | |
| C. | 冷冻海水使之结冰,从而使盐分分离出来 | |
| D. | 利用只允许水通而不允许水中溶解的物质透过的半透膜,将海水和淡水分隔开 |
12.铝合金是工业中应用最广泛的一类有色金属结构材料,在航空、航天、汽车、机械制造、船舶及化学工业中已大量应用.工业经济的飞速发展,对铝合金的需求日益增多,使铝合金的研究也随之深入.已知某合金粉末除铝外,还含有铁、铜中的一种或两种.某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.
查阅资料:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有铜(填名称).
猜想3:该合金粉末中除铝外,还含有铁、铜.
实验探究:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
探究结论:猜想3成立.
反思:一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式2Al+6HCl═2AlCl3+3H2↑.
查阅资料:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有铜(填名称).
猜想3:该合金粉末中除铝外,还含有铁、铜.
实验探究:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的30% NaOH溶液,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有铝. |
| ②取步骤①所得滤渣,加过量的10% 盐酸,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有铁和铜. |
反思:一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式2Al+6HCl═2AlCl3+3H2↑.
19.下列有关实验操作正确或能达到预期目的是( )
| A. |  点燃酒精灯 | B. |  制备并检验氢气的可燃性 | ||
| C. |  海带灼烧成灰 | D. |  液体加热 |
 ”、“
”、“ ”、“
”、“ ”表示核电荷数不同的原子,其中能用来表示混合物的是①C;能表示3H2的是②B(填图下字母,下同)能用来表示氧化物的是③A.能用来表示铁这种物质的是④D.
”表示核电荷数不同的原子,其中能用来表示混合物的是①C;能表示3H2的是②B(填图下字母,下同)能用来表示氧化物的是③A.能用来表示铁这种物质的是④D.

