题目内容
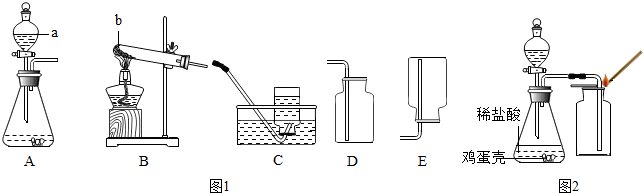
钙鸡蛋壳的主要成分是碳酸钙,为了测定某鸡蛋壳中碳酸钙的质量分数,某同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g 放在烧杯里,然后往烧杯中加入足量的稀盐酸90g,充分反应后,称得烧杯中物质的总质量为97.8g.(假设其他物质不与盐酸反应)
(1)产生二氧化碳气体 g.
(2)计算该鸡蛋壳中碳酸钙的质量分数,要求写出完整的解题步骤.
(1)产生二氧化碳气体
(2)计算该鸡蛋壳中碳酸钙的质量分数,要求写出完整的解题步骤.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据反应前后的质量差,可以计算生成二氧化碳的质量;
(2)碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据生成二氧化碳的质量,可以计算碳酸钙的质量,从而可以计算鸡蛋壳中碳酸钙的质量分数.
(2)碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据生成二氧化碳的质量,可以计算碳酸钙的质量,从而可以计算鸡蛋壳中碳酸钙的质量分数.
解答:解:(1)生成的二氧化碳质量为:10g+90g-97.8g=2.2g;故填:2.2;
(2)设该鸡蛋壳中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 2.2g
=
x=5g
该鸡蛋壳中碳酸钙的质量分数
×100%=50%
答:该鸡蛋壳中碳酸钙的质量分数为50%.
(2)设该鸡蛋壳中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 2.2g
| 100 |
| x |
| 44 |
| 2.2g |
x=5g
该鸡蛋壳中碳酸钙的质量分数
| 5g |
| 10g |
答:该鸡蛋壳中碳酸钙的质量分数为50%.
点评:学会利用差量法计算二氧化碳的质量,同时应注意解答步骤的规范性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列家庭酿制葡萄酒的过程中属于化学变化的是( )
| A、清洗葡萄 |
| B、把葡萄捣碎 |
| C、用细纱布过滤后装瓶 |
| D、葡萄发酵成酒 |
下列化学式的读法和写法均正确的是( )
| A、氧气:O |
| B、氧化铝:Al3O2 |
| C、氯化钠:NaCl |
| D、氢氧化镁:MgOH |
在化学反应前后,可能会改变的是( )
| A、分子的种类 |
| B、原子的数目 |
| C、元素的种类 |
| D、分子的数目 |