题目内容
17.请根据如图所示的实验过程和提供的数据,回答以下问题.
(1)过程②中产生气体的原因是(用化学方程式表示)Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(2)计算过程①中消耗碳酸钠固体的质量.(写出计算过程,结果保留一位小数).
(3)计算溶液A的质量(写出计算过程,结果保留一位小数).
分析 (1)根据图示②中加入碳酸钠后又生成了气体,说明①中加入盐酸是过量的
(2)根据6.6g气体的质量求出①中消耗碳酸钠固体的质量;
(3)根据化学反应的方程式,结合溶质的质量分数计算公式来分析解答
解答 解:(1)由图示②中加入碳酸钠后又生成了气体,说明①中加入盐酸是过量的;即100g溶液中含有的溶质既有碳酸钠与盐酸反应生成的氯化钠,又有过量的氯化氢,化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑;
故填:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(2)设①中消耗的碳酸钠的质量为m1.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
m1 6.6 g
$\frac{106}{m1}=\frac{44}{6.6g}$
m1=15.9g
答:过程①中消耗碳酸钠固体的质量是15.9g;
(3)设②中消耗的碳酸钠的质量为m2
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
m2 2.2g
$\frac{106}{m2}=\frac{44}{2.2g}$
m2=5.3g
m(溶液A)=100 g+15.9 g+5.3 g-(6.6 g+2.2 g)=112.4g
答:溶液A的质量为112.4 g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
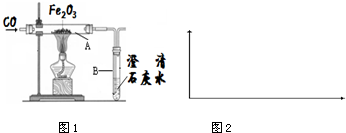
6.某化学兴趣小组如图1模拟教材中的炼铁实验,再将所得的黑色粉末物质与足量的稀硫酸反应,发现黑色粉末消失,但始终没有气泡生成.
(1)铁元素的常见价态有+2、+3.将Fe3O4表示为两种氧化物的结合形式FeO•Fe2O3.
(2)根据现象“没有气泡生成”猜想,黑色粉末物质可能是:
①氧化亚铁;②四氧化三铁;③氧化亚铁和四氧化三铁的混合物.
(3)图中装置有明显缺陷,从环保角度出发,应采取的措施是将尾气点燃.
(4)从实验安全角度考虑,应在装置A、B间增加一个安全瓶,可以有效防止B中的澄清石灰水倒吸入A中.
(5)某科技小组查阅CO与Fe2O3反应各产物开始生成的温度情况:
Fe2O3$\stackrel{300℃以上}{→}$Fe3O4$\stackrel{600℃以上}{→}$FeO$\stackrel{700℃以上}{→}$Fe
由于酒精灯通常只能提供400-500℃的温度,则黑色粉末的成分理论上可确定为Fe3O4.
(6)设计实验对黑色粉末进行探究.
某同学选用X溶液与黑色粉末反应,也可以证明黑色粉末中不含有Fe,则X为A.
A.硫酸铜溶液 B.硫酸钠溶液 C.氢氧化钠溶液 D.氢氧化钙溶液
(7)在一定温度下,该科研小组将3.2克Fe2O3与足量的CO混合加热,反应结束后冷却,精确称量黑色粉末质量为ag(计算保留两位有效数字)
①若a=2.24g,黑色粉末是Fe;②若a=2.88g,黑色粉末是FeO;③若a=3.09g,黑色粉末是Fe3O4;
④若黑色粉末是混合物则a的取值范围是2.24g<a<3.09g.
(8)请你画出以温度为横坐标,玻璃管中剩余固体的质量为纵坐标(如图2),表示用CO还原Fe2O3.

(1)铁元素的常见价态有+2、+3.将Fe3O4表示为两种氧化物的结合形式FeO•Fe2O3.
(2)根据现象“没有气泡生成”猜想,黑色粉末物质可能是:
①氧化亚铁;②四氧化三铁;③氧化亚铁和四氧化三铁的混合物.
(3)图中装置有明显缺陷,从环保角度出发,应采取的措施是将尾气点燃.
(4)从实验安全角度考虑,应在装置A、B间增加一个安全瓶,可以有效防止B中的澄清石灰水倒吸入A中.
(5)某科技小组查阅CO与Fe2O3反应各产物开始生成的温度情况:
Fe2O3$\stackrel{300℃以上}{→}$Fe3O4$\stackrel{600℃以上}{→}$FeO$\stackrel{700℃以上}{→}$Fe
由于酒精灯通常只能提供400-500℃的温度,则黑色粉末的成分理论上可确定为Fe3O4.
(6)设计实验对黑色粉末进行探究.
| 操作步骤 | 实验现象 | 解释或反应方程式 |
| 1.取少量黑色物质加入 30%热的盐酸中 | 无气泡、溶液颜 色变成黄绿色 | 该反应的化学方程式:Fe3O4+8HCl═FeCl2+2FeCl3+4H2O |
| 2.用磁铁吸引此粉末 | 能够被吸引 | 说明该物质具有磁性 |
A.硫酸铜溶液 B.硫酸钠溶液 C.氢氧化钠溶液 D.氢氧化钙溶液
(7)在一定温度下,该科研小组将3.2克Fe2O3与足量的CO混合加热,反应结束后冷却,精确称量黑色粉末质量为ag(计算保留两位有效数字)
①若a=2.24g,黑色粉末是Fe;②若a=2.88g,黑色粉末是FeO;③若a=3.09g,黑色粉末是Fe3O4;
④若黑色粉末是混合物则a的取值范围是2.24g<a<3.09g.
(8)请你画出以温度为横坐标,玻璃管中剩余固体的质量为纵坐标(如图2),表示用CO还原Fe2O3.
7.下列各组内物质的溶液混合后,所得溶液一定呈碱性的是( )
| A. | KOH、Na2CO3、HCl | B. | BaCl2、NaCl、H2SO4 | ||
| C. | Ca(OH)2、KNO3、Na2CO3 | D. | Ba(OH)2、NaOH、HNO3 |
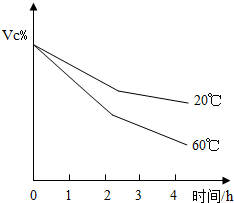 兴趣小组的同学对食品中含有的维生素C(化学式为C6H8O6,可表示为Vc)进行探究.
兴趣小组的同学对食品中含有的维生素C(化学式为C6H8O6,可表示为Vc)进行探究.