题目内容
 如图是某葡萄糖酸锌口服液的标签.根据题意回答:
如图是某葡萄糖酸锌口服液的标签.根据题意回答:(1)标签上的含锌6.5mg是指
A.单质 B.元素 C.分子 D.原子
(2)每个葡萄糖酸锌分子中共有
(3)葡萄糖酸锌的相对分子质量是455,每支该口服液中葡萄糖酸锌的质量是多少(要求有计算过程).
考点:标签上标示的物质成分及其含量,元素的概念,化学式的书写及意义,化合物中某元素的质量计算
专题:标签图示型
分析:(1)欲正确解答本题,须知化学式的概念.
(2)欲正确解答本题,须知分子的原子个数等于组成该物质的元素个数的总和.
(3)欲正确解答本题,须先根据元素的质量分数公式计算出葡萄糖酸锌中的锌的质量分数,然后运用质量分数公式计算出每支该口服液中葡萄糖酸锌的质量.
(2)欲正确解答本题,须知分子的原子个数等于组成该物质的元素个数的总和.
(3)欲正确解答本题,须先根据元素的质量分数公式计算出葡萄糖酸锌中的锌的质量分数,然后运用质量分数公式计算出每支该口服液中葡萄糖酸锌的质量.
解答:解:(1)含锌6.5mg是指葡萄糖酸锌分子中所含锌元素的质量.故选B.
(2)葡萄糖酸锌的化学式是C12H22O14Zn,原子个数为:12+22+14+1=49,故答案为:49.
(3)葡萄糖酸锌中的锌的质量分数为
×100%≈14.3%
每支该口服液中葡萄糖酸锌的质量为:6.5mg÷14.3%≈45.5mg
答案:
(1)B
(2)49
(3)每支该口服液中葡萄糖酸锌的质量是45.5mg
(2)葡萄糖酸锌的化学式是C12H22O14Zn,原子个数为:12+22+14+1=49,故答案为:49.
(3)葡萄糖酸锌中的锌的质量分数为
| 65 |
| 455 |
每支该口服液中葡萄糖酸锌的质量为:6.5mg÷14.3%≈45.5mg
答案:
(1)B
(2)49
(3)每支该口服液中葡萄糖酸锌的质量是45.5mg
点评:本题主要考查学生对化学式的概念的认识,以及对分子中原子个数的计算方法的掌握情况,运用质量分数公式进行计算的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
如图是CO与CuO反应的装置,下列关于图示实验说法正确的是( )
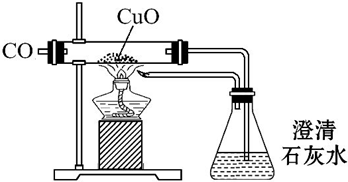
①说明CO具有还原性
②玻璃管中黑色固体变成了红色固体
③说明CO被还原后的产物是CO2
④既有效地防止了CO对空气的污染,又充分利用了能源
⑤玻璃管中发生的反应为置换反应.

①说明CO具有还原性
②玻璃管中黑色固体变成了红色固体
③说明CO被还原后的产物是CO2
④既有效地防止了CO对空气的污染,又充分利用了能源
⑤玻璃管中发生的反应为置换反应.
| A、①②④ | B、①③④ |
| C、①④⑤ | D、全部正确 |
二氧化碳的下列用途中,仅仅是利用二氧化碳物理性质的是( )
| A、二氧化碳供植物光合作用 |
| B、二氧化碳制成干冰作致冷剂 |
| C、将二氧化碳溶于水制汽水 |
| D、液态二氧化碳作灭火剂 |
下列关于燃烧现象的描述,正确的是( )
| A、硫在氧气中燃烧产生大量的白烟 |
| B、红磷在空气中燃烧发出蓝紫色火焰 |
| C、木炭在空气中燃烧发出耀眼的白光 |
| D、细铁丝在氧气中剧烈燃烧,火星四射 |
现有镁、铝两种金属分别跟稀盐酸充分反应,生成相同质量的氢气.则可能的情况有( )
| A、足量的稀盐酸与等质量的镁、铝分别发生反应 |
| B、足量的稀盐酸与质量比为4:3的镁、铝分别发生反应 |
| C、足量的稀盐酸与质量比为8:9的镁、铝分别发生反应 |
| D、等质量的同一种稀盐酸与过量的镁、铝分别发生反应 |
下列物质中,能跟BaCl2、Al2O3、(NH4)2CO3都发生反应的是( )
| A、CO2 |
| B、H2SO4 |
| C、CuSO4 |
| D、KOH |
