题目内容
 数字化装备正逐步进入宜昌市的各个校园.在盐酸和氢氧化钠反应的过程中,如图是利用数字化传感器得到的溶液pH变化图象.
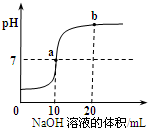
数字化装备正逐步进入宜昌市的各个校园.在盐酸和氢氧化钠反应的过程中,如图是利用数字化传感器得到的溶液pH变化图象.(1)反应的化学方程式为
(2)当溶液呈中性时,所消耗氢氧化钠溶液的体积是
(3)图中b点所示溶液中,含有的溶质是
考点:中和反应及其应用,溶液的酸碱性与pH值的关系,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:(1)根据氢氧化钠和盐酸反应生成氯化钠和水进行分析;
(2)根据图象中的关键点进行分析;
(3)根据b点时,溶液显碱性,氢氧化钠过量,碱能使酚酞变红色进行分析.
(2)根据图象中的关键点进行分析;
(3)根据b点时,溶液显碱性,氢氧化钠过量,碱能使酚酞变红色进行分析.
解答:解:(1)氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:NaOH+HCl=NaCl+H2O;
(2)由图示,当溶液呈中性时,pH=7,此时所消耗氢氧化钠溶液的体积是10mL;
(3)b点时,溶液显碱性,氢氧化钠过量,含有的溶质是NaOH和NaCl,滴入几滴酚酞溶液,可观察到现象为:溶液变红色.
故答案为:(1)NaOH+HCl═NaCl+H2O;
(2)10;
(3)NaOH和NaCl,溶液变红色.
(2)由图示,当溶液呈中性时,pH=7,此时所消耗氢氧化钠溶液的体积是10mL;
(3)b点时,溶液显碱性,氢氧化钠过量,含有的溶质是NaOH和NaCl,滴入几滴酚酞溶液,可观察到现象为:溶液变红色.
故答案为:(1)NaOH+HCl═NaCl+H2O;
(2)10;
(3)NaOH和NaCl,溶液变红色.
点评:在解此类题时,会正确分析图象中的关键点是正确解决问题的关键.

练习册系列答案
相关题目
下列粒子结构示意图中,表示阳离子的是( )
A、 |
B、 |
C、 |
D、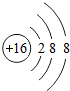 |
下列结构示意图表示的微粒中,最易得到电子的是( )
A、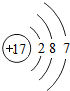 |
B、 |
C、 |
D、 |
下列实验现象描述与事实不符合的是( )
| A、水通电一段时间后,得到的氧气与氢气在相同条件下体积比约为1:2 |
| B、木炭在氧气中燃烧,发出白光,生成一种使澄清石灰水变浑浊的气体 |
| C、镁与稀盐酸反应产生气泡,溶液由无色变成浅绿色 |
| D、氢气燃烧发出淡蓝色火焰,放出大量的热 |
化学实验操作的正确性、规范性是科学探究成败的关键因素之一.下列实验操作中,正确的是( )
A、 加热液体 |
B、 塞紧橡皮塞 |
C、 稀释浓硫酸 |
D、 测定溶液的pH 测定溶液的pH |


 冷水
冷水
 硅元素在现代信息技术产业有着广泛的应用,如图摘自元素周期表,请你将如图能提供的关于硅元素的信息
硅元素在现代信息技术产业有着广泛的应用,如图摘自元素周期表,请你将如图能提供的关于硅元素的信息