题目内容
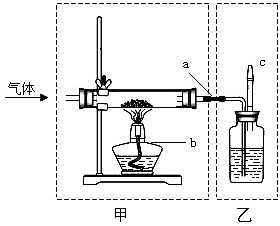 利用如图装置可进行气体性质的探究实验.甲的玻璃管中盛放黑色粉末(CuO或C),乙的洗气瓶中盛放无色溶液(澄清石灰水或NaOH溶液).
利用如图装置可进行气体性质的探究实验.甲的玻璃管中盛放黑色粉末(CuO或C),乙的洗气瓶中盛放无色溶液(澄清石灰水或NaOH溶液).(1)根据要求填表:
| 实验 | 甲 | 乙 |
| 实验一:探究CO与 CuO的反应. |
反应的化学方程式: 还原剂: |
澄清石灰水的作用: |
| 实验二:探究CO2与 C的反应. (b换成酒精喷灯) |
反应的化学方程式: 反应类型: |
NaOH溶液的作用: |
(3)实验一中观察到的现象:
(4)实验一反应结束,先将a处断开,再停止加热,这样做的目的是
(5)上述两实验中,在导管c的尖嘴处都用火柴点燃,其目的是否完全相同?简述理由
考点:一氧化碳的化学性质,气体的净化(除杂),二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:碳单质与含碳化合物的性质与用途
分析:(1)实验一:熟记CO与CuO的反应的化学反应式;化学反应中失去氧的物质是氧化剂;二氧化碳与澄清石灰水变浑浊;
实验二:熟记CO2与C的反应的化学反应式;熟悉四种反应类型;氢氧化钠溶液可吸收二氧化碳气体;
(2)依据可燃性气体加热或点燃时容易发生爆炸分析解答;
(3)根据一氧化碳还原氧化铜的现象解答;
(4)根据若先停止加热乙中的液体会倒吸炸裂玻璃管解答;
(5)根据一氧化碳具有可燃性,燃烧生成二氧化碳解答.
实验二:熟记CO2与C的反应的化学反应式;熟悉四种反应类型;氢氧化钠溶液可吸收二氧化碳气体;
(2)依据可燃性气体加热或点燃时容易发生爆炸分析解答;
(3)根据一氧化碳还原氧化铜的现象解答;
(4)根据若先停止加热乙中的液体会倒吸炸裂玻璃管解答;
(5)根据一氧化碳具有可燃性,燃烧生成二氧化碳解答.
解答:解:(1)实验一:在加热的条件下,一氧化碳与氧化铜反应生成了二氧化碳和铜,反应的方程式是:CO+CuO
Cu+CO2.在反应中,一氧化碳得到了氧,是还化剂.由于二氧化碳能与氢氧化钙反应生成白色沉淀,现象明显.所以,澄清石灰水的作用:检验有二氧化碳气体生成.
实验二:在高温条件下,CO2和C的反应生成了一氧化碳,反应的方程式是:C+CO2
2CO;该反应由两种物质生成了一种物质,属于化合反应.由于二氧化碳能与氢氧化钠反应.所以,NaOH溶液的作用:吸收二氧化碳气体.所以,填表如下::
(2)根据CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此,应先通CO排尽玻璃管中的空气,然后再加热.所以在该实验中先通CO气体的作用是:排净装置中的空气,防止CO和装置中的空气混合受热发生爆炸;
故答案:排尽试管内的空气,防止CO与空气混合点燃时发生爆炸;
(3)一氧化碳还原氧化铜生成铜和二氧化碳,黑色固体逐渐变红,澄清石灰水变浑浊;
故答案:黑色固体逐渐变红,澄清石灰水变浑浊;
(4)若先停止加热乙中的液体会倒吸炸裂玻璃管,
故答案:防止停止加热后,石灰水倒流将热玻璃管骤冷炸裂;
(5)实验一是利用一氧化碳燃烧生成二氧化碳除去一氧化碳;实验二是为了验证碳和二氧化碳反应生成一氧化碳,
故答案:不完全相同;实验一的目的是除去有毒的CO尾气,防止污染;实验二的主要目的是证明高温下CO2与C能反应,且产物是CO.
| ||
实验二:在高温条件下,CO2和C的反应生成了一氧化碳,反应的方程式是:C+CO2
| ||
| 实验一 探究CO和CuO的反应 |
反应的化学方程式: CO+CuO
氧化剂:氧化铜 |
澄清石灰水的作用: 检验有二氧化碳气体生成 | ||||
| 实验二 探究CO2和C的反应(b换成酒精喷灯) |
反应的化学方程式: C+CO2
基本反应类型 化合反应 |
NaOH溶液的作用: 吸收二氧化碳气体 |
故答案:排尽试管内的空气,防止CO与空气混合点燃时发生爆炸;
(3)一氧化碳还原氧化铜生成铜和二氧化碳,黑色固体逐渐变红,澄清石灰水变浑浊;
故答案:黑色固体逐渐变红,澄清石灰水变浑浊;
(4)若先停止加热乙中的液体会倒吸炸裂玻璃管,
故答案:防止停止加热后,石灰水倒流将热玻璃管骤冷炸裂;
(5)实验一是利用一氧化碳燃烧生成二氧化碳除去一氧化碳;实验二是为了验证碳和二氧化碳反应生成一氧化碳,
故答案:不完全相同;实验一的目的是除去有毒的CO尾气,防止污染;实验二的主要目的是证明高温下CO2与C能反应,且产物是CO.
点评:本题主要考查了碳及其化合物的有关性质,涉及到了化学方程式的书写和实验操作分析等知识.对于实验中CO的尾气吸收、二氧化碳的检验都是实验题中常考知识点.

练习册系列答案
相关题目
 现有A~G七种物质,已知A是赤铁矿的主要成分,B是一种气体,E的浓溶液加水稀释时会放出大量的热,G溶液为蓝色,它们之间存在如图所示的转化关系:
现有A~G七种物质,已知A是赤铁矿的主要成分,B是一种气体,E的浓溶液加水稀释时会放出大量的热,G溶液为蓝色,它们之间存在如图所示的转化关系:
 小琳取了一块石灰石(杂质既不溶于水也不与盐酸反应).将其敲打粉碎后,称出一定质量的样品放入烧杯内,然后加入50g稀盐酸,恰好完全反应.反应所需时间(t)和烧杯及其所盛物质的总质量(m)的关系如图所示.(烧杯质量为18g).
小琳取了一块石灰石(杂质既不溶于水也不与盐酸反应).将其敲打粉碎后,称出一定质量的样品放入烧杯内,然后加入50g稀盐酸,恰好完全反应.反应所需时间(t)和烧杯及其所盛物质的总质量(m)的关系如图所示.(烧杯质量为18g).