题目内容
18.下列金属制品中,利用金属导电性的是( )| A. | 铝箔 | B. | 铁锅 | C. | 铜导线 | D. | 金项链 |
分析 物质的性质决定物质的用途,根据金属的物理性质与用途,进行分析解答.
解答 解:A、铝箔,是利用了铝具有良好的延展性,故选项错误.
B、铁锅,是利用了铁具有良好的导热性,故选项错误.
C、铜导线,是利用了铜具有良好的导电性,故选项正确.
D、金项链,是利用了黄金性质稳定、色泽好的性质,故选项错误.
故选:C.
点评 本题难度不大,物质的性质决定物质的用途,掌握常见金属的性质和用途是正确解答此类题的关键.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
8.某化学实验活动小组的同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验.请你参与他们进行的探究活动:
提出问题:久置氢氧化钠固体的成分是什么?
猜想与假设:
猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;猜想Ⅲ:NaOH和Na2CO3.
实验与探究:
(1)实验如表:
(2)为了进一步的验证猜想结果,小明同学提出如下实验方案:继续步骤二的实验,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想Ⅲ成立;若酚酞不变红,则猜想Ⅱ成立.
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈碱性(填“酸”或“碱”),能使酚酞变红,因此他认为该方案的操作步骤中应该改进的是滴加过量的氯化钡溶液.
反思与交流:
久置的固体氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH═Na2CO3+H2O.
提出问题:久置氢氧化钠固体的成分是什么?
猜想与假设:
猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;猜想Ⅲ:NaOH和Na2CO3.
实验与探究:
(1)实验如表:
| 实验操作步骤 | 实验现象 | 结论及解释 |
| 步骤一:取少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的稀盐酸. | 实验过程中始终没有气泡产生. | 则证明猜想Ⅰ成立. |
| 步骤二:另取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加氯化钡溶液. | 实验过程中产生白色沉淀. | 则证明猜想Ⅱ或Ⅲ成立. |
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈碱性(填“酸”或“碱”),能使酚酞变红,因此他认为该方案的操作步骤中应该改进的是滴加过量的氯化钡溶液.
反思与交流:
久置的固体氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH═Na2CO3+H2O.
9.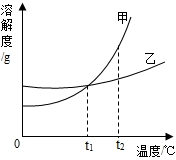 甲、乙两种固体的溶解度曲线如图所示.下列有关叙述中错误的是( )
甲、乙两种固体的溶解度曲线如图所示.下列有关叙述中错误的是( )
 甲、乙两种固体的溶解度曲线如图所示.下列有关叙述中错误的是( )
甲、乙两种固体的溶解度曲线如图所示.下列有关叙述中错误的是( )| A. | t2℃时甲的溶解度比乙大 | |
| B. | 将相等质量的甲、乙两物质的饱和溶液温度从t2℃降到t1℃,析出的甲固体质量比乙固体质量大 | |
| C. | 升高温度可将甲的饱和溶液变为不饱和溶液 | |
| D. | t2℃时,甲和乙的饱和溶液各100g,其中溶质的质量相等 |
13. 三种不含结晶水的固体物质A、B、C的溶解度曲线如图,下列说法中正确的是( )
三种不含结晶水的固体物质A、B、C的溶解度曲线如图,下列说法中正确的是( )
 三种不含结晶水的固体物质A、B、C的溶解度曲线如图,下列说法中正确的是( )
三种不含结晶水的固体物质A、B、C的溶解度曲线如图,下列说法中正确的是( )| A. | 在t2℃时,A、B两物质的溶解度相等 | |
| B. | 在t1℃时,三种物质的溶解度由大到小的顺序是A>B>C | |
| C. | A、B、C三种物质的饱和溶液升温都会转化为不饱和溶液 | |
| D. | 要从含有少量B的A溶液中得到较多的B晶体,通常可采用降温结晶的方法 |
10. 小灵设计了如图所示的趣味实验装置,其气密性良好.若要使B中长导管下端有气泡出现,则A中加入的固体和液体可能是( )
小灵设计了如图所示的趣味实验装置,其气密性良好.若要使B中长导管下端有气泡出现,则A中加入的固体和液体可能是( )
 小灵设计了如图所示的趣味实验装置,其气密性良好.若要使B中长导管下端有气泡出现,则A中加入的固体和液体可能是( )
小灵设计了如图所示的趣味实验装置,其气密性良好.若要使B中长导管下端有气泡出现,则A中加入的固体和液体可能是( )| A. | 氢氧化钠固体和稀硫酸 | B. | 硝酸铵和水 | ||
| C. | 二氧化锰和过氧化氢溶液 | D. | 铜和稀硫酸 |
8. 甲乙两种物质(均不含结晶水)的溶解度曲线如图,下列说法正确的是( )
甲乙两种物质(均不含结晶水)的溶解度曲线如图,下列说法正确的是( )
 甲乙两种物质(均不含结晶水)的溶解度曲线如图,下列说法正确的是( )
甲乙两种物质(均不含结晶水)的溶解度曲线如图,下列说法正确的是( )| A. | 甲和乙的溶解度相等,都等于30g | |
| B. | a2℃时甲溶液中的溶质质量一定大于乙 | |
| C. | a1℃到a2℃之间甲溶液的质量分数比乙溶液的溶质质量分数大 | |
| D. | 甲乙的不饱和溶液,从a2℃降温至a1℃,都有可能变为饱和溶液 |
 人类生产和生活都离不开金属,早在春秋战国时期,我国就开始生产和使用金属.现在,抚顺也进入了高铁时代,高铁建设需要大量的钢铁,那钢铁是字样炼成和使用的呢?主要反应过程如图所示.
人类生产和生活都离不开金属,早在春秋战国时期,我国就开始生产和使用金属.现在,抚顺也进入了高铁时代,高铁建设需要大量的钢铁,那钢铁是字样炼成和使用的呢?主要反应过程如图所示.