题目内容
2.粗盐提纯实验和配制一定溶质质量分数的氯化钠溶液实验中,下列操作正确的是( )| A. |  | B. |  | C. |  | D. |  |
分析 提纯含有少量不溶性杂质的粗盐的操作步骤为溶解、过滤、蒸发;配制一定溶质质量分数的氯化钠溶液的操作步骤为计算、称量、溶解.据此,对图示的操作进行排序.
解答 解:A、托盘天平应该左物右码,错误;
B、取药品时,瓶塞倒放,错误;
C、量筒读数是正确的;
D、不能用手拿坩埚,以免烫伤,错误;
故选C
点评 在使用固体溶解配制溶液时,操作步骤为计算-称量-溶解,其中称量包括称取溶质质量和量取溶剂体积,两个操作应先称取溶质再量取溶剂.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
12.下列食物中富含蛋白质的是( )
| A. | 米饭 | B. | 鸡蛋 | C. | 酸豆角 | D. | 苹果 |
13.厨房中报警器检测到煤气泄漏,从分子性质角度解释,这是利用( )
| A. | 分子很小 | B. | 分子在不断地运动 | ||
| C. | 分子之间有间隙 | D. | 分子可以再分 |
10.如图是钠元素和氯元素在元素周期表中的信息和有关的4种粒子结构示意图.下列说法正确的是( )
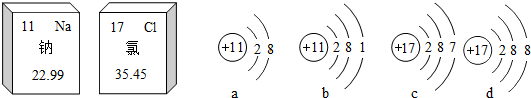
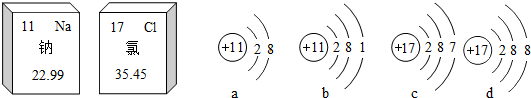
| A. | 钠、氯都属于金属元素 | B. | 氯化钠是由a、d两种粒子构成的 | ||
| C. | 氯的相对原子质量是35.45g | D. | a表示的是一种阴离子 |
17.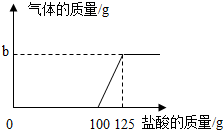 在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题.
在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题.
(1)a的数值为125,兴趣小组的同学通过实验,得出该试剂已部分变质的结论,其依据是(通过实验数据和图象做出你的分析)滴加盐酸至100g时,开始时有二氧化碳生成,证明有碳酸钙存在,之前滴加的盐酸无现象,说明了盐酸与氢氧化钙反应,从而证明氢氧化钙存在.
(2)b的数值为2.2.计算该试剂中氢氧化钙的质量分数(写出计算过程,结果保留一位小数).
 在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题.
在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题.| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入盐酸的质量(g) | 25 | 25 | 25 | 25 | 25 | 25 |
| 锥形瓶中物质的质量(g) | 75 | 100 | a | 150 | 172.8 | 197.8 |
(2)b的数值为2.2.计算该试剂中氢氧化钙的质量分数(写出计算过程,结果保留一位小数).
7. 甲、乙两种物质的溶解度曲线如图所示.下列说法中正确的是( )
甲、乙两种物质的溶解度曲线如图所示.下列说法中正确的是( )
 甲、乙两种物质的溶解度曲线如图所示.下列说法中正确的是( )
甲、乙两种物质的溶解度曲线如图所示.下列说法中正确的是( )| A. | t1℃时,甲饱和溶液的溶质质量分数大于乙饱和溶液 | |
| B. | t2℃时,甲、乙饱和溶液的溶质质量分数都为30% | |
| C. | t2℃时,甲、乙的饱和溶液分别降温至t1℃,甲溶液饱和,乙溶液不饱和 | |
| D. | t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达饱和状态,需加入甲的质量大于乙 |
2.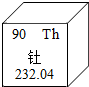 钍将可能取代汽油成为汽车的动力来源,钍元素的相关信息如图.下列有关钍的说法正确的是( )
钍将可能取代汽油成为汽车的动力来源,钍元素的相关信息如图.下列有关钍的说法正确的是( )
 钍将可能取代汽油成为汽车的动力来源,钍元素的相关信息如图.下列有关钍的说法正确的是( )
钍将可能取代汽油成为汽车的动力来源,钍元素的相关信息如图.下列有关钍的说法正确的是( )| A. | 原子的中子数是90 | B. | 属于非金属元素 | ||
| C. | 原子核外电子数是90 | D. | 相对原子质量为232.04g |
19.除去下列物质中的杂质,选用的方法或试剂正确的是( )
| 选项 | 物质 | 杂质 | 除去杂质所用的试剂和方法 |
| A | 氯化铁溶液 | 氯化铜 | 加足量铁粉 过滤 |
| B | 二氧化碳 | 氧气 | 点燃混合气体 |
| C | 铁 | 氧化铁 | 加足量盐酸 蒸发 |
| D | 碳酸钠粉末 | 碳酸钙粉末 | 加足量水 过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
20.人体内的下列体液中,呈酸性的是( )
| A. | 血浆(pH 7.35~7.45) | B. | 胆汁(pH 7.1~7.3) | ||
| C. | 胃液(pH 0.9~1.5) | D. | 胰液(pH 7.5~8.0) |