题目内容
甲、乙两同学共用一套实验装置(见图)测定铜和氧化铜混合物中铜元素的含量.虽然两位同学用的是同一套实验装置,但是具体的做法却不尽相同.甲同学关注的重点是装置D中放置固体混合物的玻管.他通过称量,测定出该玻管(含固体混合物,下同)在反应前后的质量差,然后据此计算铜的含量.而乙同学则是测定反应前后U形干燥管E(含干燥剂,下同)的质量差,再根据这些数据计算铜的含量.设试样的质量为W,反应前后玻管的质量分别为D1、D2;反应前后U形干燥管的质量分别为E1、E2.试回答下列有关问题: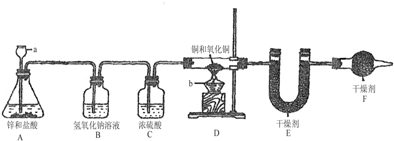
(1)写出甲、乙两同学铜元素含量的计算式:Cu%(甲)= ;Cu%(乙)= ;
(2)装置C在本实验中所起的作用是 ,如果缺少了这个装置,对实验的结果是否有影响? ;原因是: ;
(3)装置F在本实验中所起的作用是 ;如果缺少了这个装置,对实验的结果是否有影响? ;原因是: ;
(4)为保证混合物中氧化铜完全还原,实验中应该怎样操作? ;
(5)为了提高测定结果的准确性,在卸下装置D中的玻管或U形干燥管进行称量前,必须妥善地完成哪些操作? .

(1)写出甲、乙两同学铜元素含量的计算式:Cu%(甲)=
(2)装置C在本实验中所起的作用是
(3)装置F在本实验中所起的作用是
(4)为保证混合物中氧化铜完全还原,实验中应该怎样操作?
(5)为了提高测定结果的准确性,在卸下装置D中的玻管或U形干燥管进行称量前,必须妥善地完成哪些操作?
考点:实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,气体的净化(除杂),氢气的制取和检验,氢气的化学性质与燃烧实验
专题:综合实验题
分析:(1)根据D装置中减少的质量为氧化铜中氧元素的质量,而E装置中增加的质量为生成水的质量进行解答;
(2)根据浓硫酸具有吸水性进行解答;
(3)根据如不加F装置会使得空气中水蒸气进入使得水的质量增加,那么计算出的氧化铜的质量也随着增加,所以会使实验结果偏小进行解答;
(4)根据实验的注意事项进行解答;
(5)根据氢气还原氧化铜的实验步骤进行解答.
(2)根据浓硫酸具有吸水性进行解答;
(3)根据如不加F装置会使得空气中水蒸气进入使得水的质量增加,那么计算出的氧化铜的质量也随着增加,所以会使实验结果偏小进行解答;
(4)根据实验的注意事项进行解答;
(5)根据氢气还原氧化铜的实验步骤进行解答.
解答:解:(1)D装置中减少的质量为氧化铜中氧元素的质量,所以Cu%(甲)=
×100%;E装置中增加的质量为生成水的质量,所以Cu%(乙)=
×100%;故答案为:
×100%;
×100%;
(2)浓硫酸具有吸水性,所以吸收掉氢气中的水蒸气;对甲而言没有影响,但对乙的结果有影响,因为缺少了这个装置会导致E2值偏大,使铜含量的测定值偏低;C在本实验中所起的作用是吸收掉氢气的中水蒸气;对甲而言,没有影响;但对乙结果有影响,因为缺少了这个装置,会导致E2质量增加,使铜的含量测定值偏低;故答案为:吸收掉氢气的中水蒸气;对甲而言,没有影响;但对乙结果有影响;因为缺少了这个装置,会导致E2质量增加,使铜的含量测定值偏低;
(3)如不加F装置会使得空气中水蒸气进入使得水的质量增加,那么计算出的氧化铜的质量也随着增加,所以会使实验结果偏小;故答案为:吸收空气中的水蒸气;对甲而言,没有影响;但对乙结果有影响;不加F装置会使得空气中水蒸气进入使得水的质量增加,那么计算出的氧化铜的质量也随着增加,所以会使实验结果偏小;
(4)为保证混合物中氧化铜完全还原,实验中应该:多次测量D2(或E2)的值,直到前后两次的称量值相同;故填:多次测量D2(或E2)的值,直到前后两次的称量值相同;
(5)为了提高测定结果的准确性,在卸下装置D中的玻管或U形干燥管进行称量前,必须妥善地完成以下操作:熄灭酒精灯,继续通入氢气,等到D装置冷却.故填:熄灭酒精灯,继续通入氢气,等到D装置冷却.
| W-(D1-D2) |
| W |
W-(E2-E1)×
| ||
| W |
| W-(D1-D2) |
| W |
W-(E2-E1)×
| ||
| W |
(2)浓硫酸具有吸水性,所以吸收掉氢气中的水蒸气;对甲而言没有影响,但对乙的结果有影响,因为缺少了这个装置会导致E2值偏大,使铜含量的测定值偏低;C在本实验中所起的作用是吸收掉氢气的中水蒸气;对甲而言,没有影响;但对乙结果有影响,因为缺少了这个装置,会导致E2质量增加,使铜的含量测定值偏低;故答案为:吸收掉氢气的中水蒸气;对甲而言,没有影响;但对乙结果有影响;因为缺少了这个装置,会导致E2质量增加,使铜的含量测定值偏低;
(3)如不加F装置会使得空气中水蒸气进入使得水的质量增加,那么计算出的氧化铜的质量也随着增加,所以会使实验结果偏小;故答案为:吸收空气中的水蒸气;对甲而言,没有影响;但对乙结果有影响;不加F装置会使得空气中水蒸气进入使得水的质量增加,那么计算出的氧化铜的质量也随着增加,所以会使实验结果偏小;
(4)为保证混合物中氧化铜完全还原,实验中应该:多次测量D2(或E2)的值,直到前后两次的称量值相同;故填:多次测量D2(或E2)的值,直到前后两次的称量值相同;
(5)为了提高测定结果的准确性,在卸下装置D中的玻管或U形干燥管进行称量前,必须妥善地完成以下操作:熄灭酒精灯,继续通入氢气,等到D装置冷却.故填:熄灭酒精灯,继续通入氢气,等到D装置冷却.
点评:该题是一道综合实验题,实验设计严密,考查的知识点较多,解题的关键是明确实验目的和原理,分析综合装置各部分的作用.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目

 右图是某同学鉴别NH4HCO3、NH4Cl、KCl三种化肥的过程,其中试剂甲和乙分别可能是
右图是某同学鉴别NH4HCO3、NH4Cl、KCl三种化肥的过程,其中试剂甲和乙分别可能是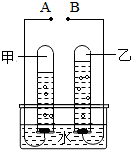 如图是电解水的实验装置图,请根据你所了解的知识填空
如图是电解水的实验装置图,请根据你所了解的知识填空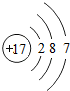 如图是氯元素的原子结构示意图,该原子的核电荷数为
如图是氯元素的原子结构示意图,该原子的核电荷数为