题目内容
16.元素周期表是我们学习化学和研究化学的重要工具.如表是元素周期表中1~18号元素原子核外电子排布,我对它进行研究:
(1)第11号元素名称是钠,它属于金属元素(填“金属”或“非金属”),它在化学反应中容易失去电子,它的离子符号为Na+.
(2)从如表中我还可以探究出以下规律:(任写两条,可从周期数,原子序数,核电荷数,核外电子数以及电子层数等的关系中考虑)
①每一周期元素的原子的核外电子层数相同;
②每一周期元素原子的最外层电子数从左到右逐渐增加.
分析 (1)原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层.若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子,若最外层电子数<4,则一般为金属元素,在化学反应中易失去电子.
(2)在元素周期表中,随原子序数的递增,原子结构中电子层数、最外层电子数发生规律性的变化,元素的种类(金属、非金属、稀有气体)等,也发生规律性的变化,据此进行分析解答.
解答 解:(1)第11号元素名称是钠,它属于金属元素,原子最外电子层上有1个电子,它在化学反应中容易失去1个电子形成阳离子,其离子符号为:Na+.故填:钠;金属;失去;Na+;
(2)每一周期元素的原子的核外电子层数相同;每一周期元素原子的最外层电子数从左到右逐渐增加;每一纵列元素原子的最外层电子数相同等.
故填:每一周期元素的原子的核外电子层数相同;每一周期元素原子的最外层电子数从左到右逐渐增加等.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息、原子结构示意图及其意义进行分析解题的能力.

练习册系列答案
相关题目
4.利用如图所示装置探究制取气体的原理、方法.

①写出仪器名称:a酒精灯,b集气瓶.
②用氯酸钾和二氧化锰的混合物制取O2,反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,选用D装置收集氧气,其原因是氧气不易溶于水;用二氧化锰和双氧水混合制氧气时,不能(填“能”或“不能”)用B装置,理由是二氧化锰是粉末.
③实验室常用氯化铵固体与碱石灰固体共热来制取一瓶易溶于水密度比空气小的氨气(NH3),应选择的装置组合是AF (填图编号).
④实验室也可用图B装置制取二氧化碳.相对于C,装置B的优点是能使反应随时进行或停止.
若用装置G来收集二氧化碳,气体应该从c端(填“c”或“d”)通入.
⑤某同学欲测定大理石中碳酸钙的质量分数.称取13.5g大理石与50.0g稀盐酸恰好反应(假设杂质不与盐酸反应,忽略盐酸的挥发),数据如下表.
根据实验数据回答下列问题:
Ⅰ.当反应时间为t6时,对应的气体质量m为4.4g;
Ⅱ.反应生成二氧化碳的物质的量为0.1 mol;
Ⅲ.计算大理石中碳酸钙的质量分数是74.1%(通过化学方程式计算,结果精确到0.1%);
Ⅳ.所用盐酸的质量分数14.6%(结果精确到0.1%).

①写出仪器名称:a酒精灯,b集气瓶.
②用氯酸钾和二氧化锰的混合物制取O2,反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,选用D装置收集氧气,其原因是氧气不易溶于水;用二氧化锰和双氧水混合制氧气时,不能(填“能”或“不能”)用B装置,理由是二氧化锰是粉末.
③实验室常用氯化铵固体与碱石灰固体共热来制取一瓶易溶于水密度比空气小的氨气(NH3),应选择的装置组合是AF (填图编号).
④实验室也可用图B装置制取二氧化碳.相对于C,装置B的优点是能使反应随时进行或停止.
若用装置G来收集二氧化碳,气体应该从c端(填“c”或“d”)通入.
⑤某同学欲测定大理石中碳酸钙的质量分数.称取13.5g大理石与50.0g稀盐酸恰好反应(假设杂质不与盐酸反应,忽略盐酸的挥发),数据如下表.
| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 气体质量m/g | 0 | 0.8 | 1.1 | 2.2 | 4.4 | 4.4 | 4.4m |
Ⅰ.当反应时间为t6时,对应的气体质量m为4.4g;
Ⅱ.反应生成二氧化碳的物质的量为0.1 mol;
Ⅲ.计算大理石中碳酸钙的质量分数是74.1%(通过化学方程式计算,结果精确到0.1%);
Ⅳ.所用盐酸的质量分数14.6%(结果精确到0.1%).
11.已知一个作为计算相对原子质量标准的碳原子的质量为m kg,一个A原子的质量为n kg,则A原子的相对原子质量为( )
| A. | $\frac{12n}{m}$ | B. | $\frac{n}{m}$ | C. | $\frac{12n}{m}$kg | D. | $\frac{n}{m}$kg |
1.关于“物质--在氧气中燃烧的主要现象--所属反应类型”描述正确的是( )
| A. | 红磷--大量白烟--化合反应 | |
| B. | 铁--火星四射--分解反应 | |
| C. | 硫--微弱的淡蓝色火焰--氧化反应 | |
| D. | 蜡烛--发出白光,瓶壁有水雾--化合反应 |
5.下列实验操作指定容器中的水,解释水的主要作用
| A | B | C | D | |
| 实 验 装 置 | 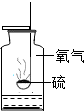 硫在氧气中燃烧 |  测定空气中氧气含量 |  铁丝在氧气中燃烧 |  探究燃烧的条件 |
| 解释 | 集气瓶中的水:吸收二氧化硫,防止污染空气 | 量筒中的水:通过水体积的变化得出O2的体积 | 集气瓶中的水:冷却溅落融化物,防止集气瓶炸裂 | 烧杯中的水:加热铜片,隔绝空气 |
