题目内容
1.铁片和铜片同时放入硝酸银溶液中,充分反应后过滤,在滤纸上留下少量滤渣A,并得到滤液B.下列关于A或B的组成说法错误的是( )(资料:HCl+AgNO3=AgCl↓+HNO3,AgCl为白色沉淀)
| A. | 若向滤渣A中滴加稀盐酸有气泡生成,则滤渣A中一定含有Ag | |
| B. | 若向滤渣A中滴加稀盐酸无气泡生成,则滤液B中可能含有Cu2+ | |
| C. | 若向滤液B中滴加稀盐酸产生白色沉淀,则滤液B中可能含有Fe2+ | |
| D. | 若向滤液B中滴加稀盐酸无明显变化,则滤渣A中一定含有Ag,可能含有Cu |
分析 根据三种金属的活动性强弱关系(铁>氢>铜>银),分析金属间的置换关系,判断溶液中含有的金属离子.
解答 解:A、向A中加入稀盐酸有气泡产生,说明铁有剩余,此时A中一定含有Ag、Cu、Fe.因此答案A正确;
B、向A中滴加稀盐酸无气泡生成,说明a中没有铁,此时B中一定含有Fe2+,可能有Cu2+,因此答案B正确;
C、向B中滴加稀盐酸产生白色沉淀,说明溶液中硝酸银溶液有剩余,但是B中一定含有Fe2+,因此答案C不正确;
D、向B中滴加稀盐酸无明显变化,说明溶液中硝酸银溶液没有剩余,即铁将银全部置换出来,因此,A中一定含有Ag,可能含有Cu,答案D正确.
故选C.
点评 金属混合粉末放入盐溶液时,活动性强的金属先与盐发生反应,待活动性强的金属完全反应后活动性弱的金属开始反应.

练习册系列答案
相关题目
11.洗涤在生活、生产中不可缺少.下列洗涤方法中利用了乳化原理的是( )
| A. | 用汽油洗去手上的油污 | B. | 用洗洁精洗去餐具上的油污 | ||
| C. | 用酒精洗去试管中的碘 | D. | 用水洗去手上的泥灰 |
12.在不用指示剂的情况下,要把含盐酸的氯化钙溶液由酸性变为中性,下列试剂可以选用的是( )
| A. | 石灰石粉末 | B. | 生灰石粉末 | C. | 澄清的石灰水 | D. | 硝酸银溶液 |
16.在蜡烛燃烧过程中,发生的变化有( )
| A. | 只有物理变化 | B. | 可能有物理变化,一定有化学变化 | ||
| C. | 只有化学变化 | D. | 既有物理变化,又有化学变化 |
6.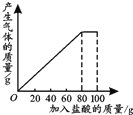 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
请计算:
(1)第2次加入盐酸后,a为25.
(2)石灰石样品中钙元素、碳元素和氧元素的质量比为10:3:22.(结果用最简整数比表示)
(3)若实验室要制备4.4g二氧化碳气体,则需要这种石灰石样品多少克?(请写出计算过程)
 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象. | 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
(1)第2次加入盐酸后,a为25.
(2)石灰石样品中钙元素、碳元素和氧元素的质量比为10:3:22.(结果用最简整数比表示)
(3)若实验室要制备4.4g二氧化碳气体,则需要这种石灰石样品多少克?(请写出计算过程)
13.下列属于同一种物质的是( )
| A. | 汞和水银 | B. | 铁和铁锈 | C. | 木材和木炭 | D. | 石墨与金刚石 |
10.人人都应关心和保护人类生存的环境.在中央电视台发布的重点城市空气质量日报中可看到,造成空气污染的首要污染物是可吸入颗粒物(粉尘)和二氧化硫.下列对其形成主要原因的分析不合理的是( )
| A. | 环境绿化不好,粉尘随风飘扬 | B. | 生活和生产中燃烧煤炭 | ||
| C. | 工业生产排放废水 | D. | 机动车排放尾气 |
11.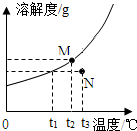 如图为X物质的溶解度曲线,M,N两点分别表示X物质溶于100g水中所形成的两种溶液.下列做法不能实现M,N间的相互转化的是(X从溶液中析出时不带结晶水)( )
如图为X物质的溶解度曲线,M,N两点分别表示X物质溶于100g水中所形成的两种溶液.下列做法不能实现M,N间的相互转化的是(X从溶液中析出时不带结晶水)( )
 如图为X物质的溶解度曲线,M,N两点分别表示X物质溶于100g水中所形成的两种溶液.下列做法不能实现M,N间的相互转化的是(X从溶液中析出时不带结晶水)( )
如图为X物质的溶解度曲线,M,N两点分别表示X物质溶于100g水中所形成的两种溶液.下列做法不能实现M,N间的相互转化的是(X从溶液中析出时不带结晶水)( )| A. | 从M→N:先将M降温到t1过滤后再将其升温至t3 | |
| B. | 从M→N:先将M恒温蒸发掉适量的水再升温到t3 | |
| C. | 从N→M:先向N中加入适量的固体X再降温到t2 | |
| D. | 从N→M:先将N降温到t2再加入适量固体X |