题目内容
(1)碳酸钠(Na2CO3)的相对分子质量为 .
(2)分子个数相同的H2O与CO2之间氧元素的质量比是 .
(3)碳酸钠中氧元素的质量分数 .
(4)53g的碳酸钠(Na2CO3)与 g硫酸钠(Na2SO4)的含钠量相同.(通过计算回答,并写出计算过程)
(2)分子个数相同的H2O与CO2之间氧元素的质量比是
(3)碳酸钠中氧元素的质量分数
(4)53g的碳酸钠(Na2CO3)与
考点:相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据分子个数相同的H2O与CO2中所含氧原子的个数比进行分析解答.
(3)根据化合物中元素的质量分数=
×100%,进行分析解答
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(2)根据分子个数相同的H2O与CO2中所含氧原子的个数比进行分析解答.
(3)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:
(1)碳酸钠(Na2CO3)的相对分子质量为23×2+12+16×3=106.
(2)分子个数相同的H2O与CO2中所含氧原子的个数比为1:2,则分子个数相同的H2O与CO2之间氧元素的质量比是(1×16):(2×16)=1:2.
(3)碳酸钠中氧元素的质量分数=
×100%≈45.3%
(4)设需要硫酸钾的质量为x,则x×
×100%=53g×
×100%,x=67g.
故答案为:
(1)106;(2)1:2;(3)45.3%;(4)67.
(1)碳酸钠(Na2CO3)的相对分子质量为23×2+12+16×3=106.
(2)分子个数相同的H2O与CO2中所含氧原子的个数比为1:2,则分子个数相同的H2O与CO2之间氧元素的质量比是(1×16):(2×16)=1:2.
(3)碳酸钠中氧元素的质量分数=
| 16×3 |
| 106 |
(4)设需要硫酸钾的质量为x,则x×
| 39×2 |
| 39×2+32+16×4 |
| 39×2 |
| 39×2+12+16×3 |
故答案为:
(1)106;(2)1:2;(3)45.3%;(4)67.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
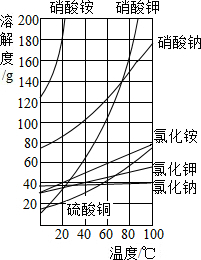 一些物质的溶解度曲线如图,回答下列问题.
一些物质的溶解度曲线如图,回答下列问题.