题目内容
7.某同学配制100g溶质质量分数为0.9%的NaCl溶液,准备了下列实验用品.回答下列问题:
(1)该同学按下列实验步骤进行:①计算 ②称量 ③量取 ④溶解(填步骤名称).
(2)配制过程还缺少的一种玻璃仪器是玻璃棒(填名称).
(3)计算所需NaCl的质量为0.9g.
分析 (1)根据配制溶质质量分数一定的溶液的基本步骤,进行分析解答.
(2)根据配制溶质质量分数一定的溶液的步骤分析解答需要的仪器,据此进行分析解答.
(3)根据溶质质量=溶液质量×溶质的质量分数,进行分析解答.
解答 解:(1)配制100g溶质质量分数为0.9%的NaCl溶液,首先计算配制溶液所需NaCl和水的质量,再称量所需的NaCl和量取水,最后进行溶解.
(2)配制100g溶质质量分数为0.9%的NaCl溶液,首先计算配制溶液所需NaCl和水的质量,再称量所需的NaCl和量取水,最后进行溶解;在这些操作中需要的仪器:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒,故还缺少的一种玻璃仪器是玻璃棒.
(3)溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为0.9%的NaCl溶液,需氯化钠的质量=100g×0.9%=0.9g.
故答案为:(1)溶解;(2)玻璃棒;(3)0.9.
点评 本题难度不大,明确一定溶质质量分数溶液的配制的步骤(计算、称量、溶解)、注意事项等是正确解答此类题的关键.

练习册系列答案
相关题目
20.现有X、Y、Z三种金属,将X、Y分别放入Z的盐溶液中,结果X表面有Z析出,Y表面无明显现象;则X、Y、Z三种金属的活动性顺序是( )
| A. | Y>Z>X | B. | X>Y>Z | C. | X>Z>Y | D. | Y>X>Z |
2.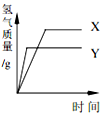 现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知X、Y在生成物中化合价均为+2价).则下列说法中正确的是( )
现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知X、Y在生成物中化合价均为+2价).则下列说法中正确的是( )
 现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知X、Y在生成物中化合价均为+2价).则下列说法中正确的是( )
现有等质量的X、Y两种金属,分别放入溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知X、Y在生成物中化合价均为+2价).则下列说法中正确的是( )| A. | 生成氢气的质量:X<Y | B. | 消耗硫酸的质量:X<Y | ||
| C. | 金属的活动性:Y<X | D. | 相对原子质量:X<Y |
16.鞍山物产丰富,下列生产过程中,只发生物理变化的是( )
| A. | 冶炼钢铁 | B. | 雕琢岫玉 | ||
| C. | 煅烧菱镁矿(MgCO3)制镁砂(MgO) | D. | 酿南果梨酒 |
17.分类是化学学习过程中常用的方法,下列分类中不正确的是( )
| A. | 单质:金刚石、液氧和铜粉 | |
| B. | 氧化物:生石灰、铁锈和“干冰” | |
| C. | 复合肥:磷酸二氢铵、磷酸氢二铵、硝酸钾 | |
| D. | 合成材料:合成纤维、塑料和合成橡胶 |

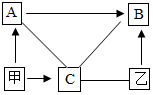 由C、H、O、Fe四种元素组成的初中常见物质间有如图所示的关系,其中A、B、C是单质,甲、乙是化合物.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质.部分反应物、生成物
由C、H、O、Fe四种元素组成的初中常见物质间有如图所示的关系,其中A、B、C是单质,甲、乙是化合物.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质.部分反应物、生成物