题目内容
某学生按下列A装置进行实验.请填写以下空白:
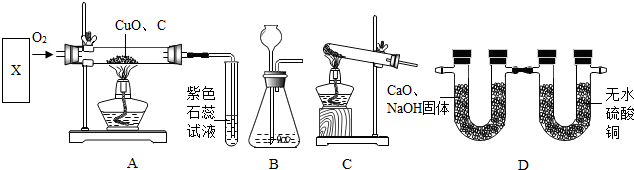
①A装置中X是制取O2的装置可用方法Ⅰ:加热氯酸钾与二氧化锰的混合物制取O2;也可用方法Ⅱ:在MnO2固体作用下分解含30%H2O2的水溶液(反应的化学方程式为2H2O2═2H2O+O2↑)制取O2.若用方法Ⅱ制取O2时,应选择 装置(填“B”或“C”).
②用方法Ⅰ制取O2时,完全反应后的固体残余物先进行 、 再往所得到的溶液中滴入少量硝酸银溶液和稀硝酸,有白色沉淀生成.证明氯酸钾中.含有 元素.
③用方法Ⅱ制取得的O2进行A图所示时,需先将其通过D装置.若无水硫酸铜不变色,说明此时得到的O2中已不含 .
④A图所示实验充分反应后,玻璃管中得到的固体物质是 .试管中出现的现象是 .

①A装置中X是制取O2的装置可用方法Ⅰ:加热氯酸钾与二氧化锰的混合物制取O2;也可用方法Ⅱ:在MnO2固体作用下分解含30%H2O2的水溶液(反应的化学方程式为2H2O2═2H2O+O2↑)制取O2.若用方法Ⅱ制取O2时,应选择
②用方法Ⅰ制取O2时,完全反应后的固体残余物先进行
③用方法Ⅱ制取得的O2进行A图所示时,需先将其通过D装置.若无水硫酸铜不变色,说明此时得到的O2中已不含
④A图所示实验充分反应后,玻璃管中得到的固体物质是
考点:氧气的制取装置,证明盐酸和可溶性盐酸盐,碳的化学性质
专题:综合实验题
分析:①制取气体的装置取决于反应物的状态和反应的条件;②根据氯酸钾的分解产物和氯离子的检验方法来分析;③根据检验水蒸气的方法来分析;④根据碳、一氧化碳的还原性来分析.
解答:解:①方法Ⅱ是用液态的过氧化氢溶液与固态的二氧化锰来制取氧气,故选择装置B;故填:B;
②氯酸钾在二氧化锰的催化作用下分解为氯化钾和氧气,其中氯化钾溶于水,二氧化锰难溶于水,故先溶解、然后过滤,向滤液中滴加硝酸银溶液和稀硝酸,会出现白色沉淀,是因为氯化钾和硝酸银反应生成氯化银白色沉淀和氯化钾;故填:溶解;过滤;氯;
③制取的氧气中含有水蒸气,通过碱石灰后得到了干燥,白色的无水硫酸铜粉末与水会变蓝色,若不变蓝,说明氧气的水蒸气已经被碱石灰完全吸收;故填:水蒸气;
④在加热的条件下,碳与氧气反应生成一氧化碳,碳和一氧化碳均能将黑色氧化铜还原为红色的金属铜.故填:铜;黑色粉末变成红色.
②氯酸钾在二氧化锰的催化作用下分解为氯化钾和氧气,其中氯化钾溶于水,二氧化锰难溶于水,故先溶解、然后过滤,向滤液中滴加硝酸银溶液和稀硝酸,会出现白色沉淀,是因为氯化钾和硝酸银反应生成氯化银白色沉淀和氯化钾;故填:溶解;过滤;氯;
③制取的氧气中含有水蒸气,通过碱石灰后得到了干燥,白色的无水硫酸铜粉末与水会变蓝色,若不变蓝,说明氧气的水蒸气已经被碱石灰完全吸收;故填:水蒸气;
④在加热的条件下,碳与氧气反应生成一氧化碳,碳和一氧化碳均能将黑色氧化铜还原为红色的金属铜.故填:铜;黑色粉末变成红色.
点评:本题考查了实验室制取氧气的原理、混合物的分离、离子的检验、以及实验现象的描述,难度适中.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
下列物质的用途中,主要应用其化学性质的是( )
| A、用铁、铝制作炊具 |
| B、铝合金用于制造门窗框架 |
| C、用酒精作燃料 |
| D、用铜制作导线 |
下列化学用语中,只能表示微观意义的是( )
①H2O ②2N ③O2 ④2H2 ⑤S2-.
①H2O ②2N ③O2 ④2H2 ⑤S2-.
| A、②④⑤ | B、②③④⑤ |
| C、①②③ | D、①②④⑤ |
下列符号中能正确表示两个钠离子的是( )
| A、Na2+ |
| B、2Na |
| C、2Na+ |
| D、Na+2 |
 水是生命之源,通过化学习,我们进一步认识到水的重要作用.
水是生命之源,通过化学习,我们进一步认识到水的重要作用. 如图是A、B两种物质的溶解度曲线,根据图示可知:
如图是A、B两种物质的溶解度曲线,根据图示可知: