题目内容
通常情况下,氯气是一种黄绿色、有刺激性气味的有毒气体,能与碱反应生成盐和水.某化学兴趣小组在实验室制取氯气,并探究氯气与石灰乳反应的条件和产物.已知:
①二氧化锰与浓盐酸反应制备氯气的反应:MnO2+4HCl
MnCl2+Cl2↑+2H2O
②氯气和石灰乳的反应:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,该反应放热.
温度较高时,氯气和石灰乳还能发生如下反应:
6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O
该兴趣小组设计了下列实验装置,进行实验.

请回答下列问题:
(1)①装置乙的作用是除去挥发出来的氯化氢气体,装置丁的作用是 .
②该兴趣小组用足量浓盐酸与8.7gMnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2 g(请写出计算过程).
(2)小组成员发现,在装置气密性良好的前提下,产物中Ca(ClO)2的质量明显小于理论值.你认为可能的原因是 .
(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进.请你给出一种改进方法: .
①二氧化锰与浓盐酸反应制备氯气的反应:MnO2+4HCl
| ||
②氯气和石灰乳的反应:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,该反应放热.
温度较高时,氯气和石灰乳还能发生如下反应:
6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O
该兴趣小组设计了下列实验装置,进行实验.

请回答下列问题:
(1)①装置乙的作用是除去挥发出来的氯化氢气体,装置丁的作用是
②该兴趣小组用足量浓盐酸与8.7gMnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2
(2)小组成员发现,在装置气密性良好的前提下,产物中Ca(ClO)2的质量明显小于理论值.你认为可能的原因是
(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进.请你给出一种改进方法:
考点:实验探究物质的性质或变化规律,气体的净化(除杂),根据化学反应方程式的计算
专题:科学探究
分析:(1)根据信息分析:饱和食盐水的主要作用是除去氯气中的氯化氢气体;氢氧化钠溶液在装置末,主要是尾气处理,防止有毒气体氯气污染环境;依据MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,结合定量关系计算理论值;
(2)根据实际的反应分析氯气反应的程度或结合信息分析氯气发生的反应等分析;
(3)依据信息反应在高温度下发生副反应,分析改进措施.
| ||
(2)根据实际的反应分析氯气反应的程度或结合信息分析氯气发生的反应等分析;
(3)依据信息反应在高温度下发生副反应,分析改进措施.
解答:解:(1)①由于氯气是有毒的气体,因此烧杯中的氢氧化钠溶液是吸收过量氯气,避免排放到空气中污染环境,进行尾气处理;
②足量的浓盐酸与8.7g MnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2;可以依据反应MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,设生成Ca(ClO)2的为x,
根据两个化学方程式,可得关系式
2MnO2~Ca(ClO)2
174 143
8.7g x
=
x=7.15g;
故答案为:进行尾气处理;7.15;
(2)在反应过程中部分氯气未与石灰乳反应而逸出导致产物中Ca(ClO)2的质量明显小于理论值或温度较高时发生了反应生成Ca(ClO)2;
故答案为:部分氯气未与石灰乳反应而逸出或温度较高时发生了反应生成Ca(ClO)2;(合理答案即可)
(3)依据信息反应在高温度下发生副反应,所以改进措施可以把丙装置放入冰水中,避免发生反应,6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O;
故答案为:将丙装置置于装有冷水的容器中.
②足量的浓盐酸与8.7g MnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2;可以依据反应MnO2+4HCl(浓)
| ||
根据两个化学方程式,可得关系式
2MnO2~Ca(ClO)2
174 143
8.7g x
| 174 |
| 143 |
| 8.7g |
| x |
故答案为:进行尾气处理;7.15;
(2)在反应过程中部分氯气未与石灰乳反应而逸出导致产物中Ca(ClO)2的质量明显小于理论值或温度较高时发生了反应生成Ca(ClO)2;
故答案为:部分氯气未与石灰乳反应而逸出或温度较高时发生了反应生成Ca(ClO)2;(合理答案即可)
(3)依据信息反应在高温度下发生副反应,所以改进措施可以把丙装置放入冰水中,避免发生反应,6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O;
故答案为:将丙装置置于装有冷水的容器中.
点评:本题考查了氯气的实验是制备和工业制备,实验过程注意问题,反应化学方程式的书写,漂白粉的制取条件,化学方程式的计算应用,题目难度中等.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
下列实验操作正确的是( )
A、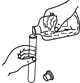 倾倒液体 |
B、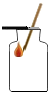 氧气验满 |
C、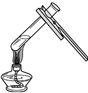 液体加热 |
D、 量9.5mL液体 |
下列物质的名称、俗名与化学式完全对应的是( )
| A、氯化钠 食盐 NaCl2 |
| B、碳酸氢钠 纯碱 NaHCO3 |
| C、氢氧化钙 熟石灰 CaO |
| D、氢氧化钠 火碱 NaOH |
区别H2、O2、CO2三种气体能够成功的方法是( )
| A、将气体分别通人灼热的CuO |
| B、将气体分别用燃着的木条试验 |
| C、将气体分别通人澄清的石灰水里 |
| D、将气体分别通过灼热的铜丝 |

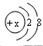 所示,则X=
所示,则X=