题目内容
12.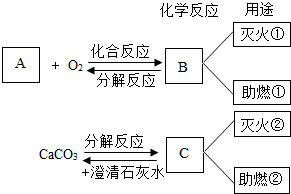 如图是A、B、C三种物质有关反应和用途的示意图,其其妙处是B、C两物质具有看似矛盾的用途.
如图是A、B、C三种物质有关反应和用途的示意图,其其妙处是B、C两物质具有看似矛盾的用途.(1)写出B的化学式:H2O
(2)写出B的灭火原理①降低温度到着火点以下;写出C的灭火原理②隔绝氧气.
(3)通过写出“--”中化学式,并在“□”中填数字,配平以下两个化学方程式:
阻燃反应①:□C+□H2O$\stackrel{高温}{→}$□+□H2
阻燃反应①:□Mg+□CO2$\stackrel{点燃}{→}$□MgO+□C
物质所处环境条件改变后,B、C两种物质由灭火剂变成了阻燃物,与此类似,反应物相同,反应条件改变,生成物截然不同的反应还有一些,请任举一例6H2O+6CO2$\frac{\underline{\;光合作用\;}}{\;}$C6H12O6+6O2.
分析 根据A和氧气化合反应生成B,B通过分解反应生成A,所以A是水,水灭火的原理是降低温度到着火点以下,二氧化碳灭火的原理是隔绝氧气,二氧化碳和水在常温条件下会生成碳酸,二氧化碳和水通过光合作用会生成葡萄糖和氧气等知识进行分析.
解答 解:(1)A和氧气化合反应生成B,B通过分解反应生成A,所以A是水,化学式为:H2O;
(2)水的灭火原理是:降低温度到着火点以下,二氧化碳的灭火原理是隔绝氧气;
(3)C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2,
2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
二氧化碳和水在常温条件下会生成碳酸,二氧化碳和水通过光合作用会生成葡萄糖和氧气,化学方程式为:6H2O+6CO2$\frac{\underline{\;光合作用\;}}{\;}$C6H12O6+6O2.
故答案为:(1)H2O;
(2)降低温度到着火点以下,隔绝氧气;
(3)C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2,
2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
6H2O+6CO2$\frac{\underline{\;光合作用\;}}{\;}$C6H12O6+6O2.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列实验操作叙述正确的是( )
| A. | 实验用剩的药品应放回原试剂瓶中 | |
| B. | 过滤时,将玻璃棒靠在三层滤纸的一边 | |
| C. | 测某酸性溶液的pH时,先用水将pH试纸润湿 | |
| D. | 把烧杯置于铁架台的铁圈上直接加热 |
20.某实验小组的同学往久置的石灰水中加入过量稀盐酸.
(1)写出发生中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O,
(2)小倩向上述剩余溶液中加入一定量的碳酸钠溶液,所得溶液中的溶质可能是什么?
猜想1:NaCl
猜想2:NaCl、HCl
猜想3:NaCl、HCl、CaCl2
猜想4:NaCl、CaCl2
猜想5:NaCl、Na2CO3(填化学式)
①经分析,小蒙认为猜想2不合理,理由是若有盐酸,则一定含有氯化钙,
②为验证其余猜想,小红做了以下实验:
(1)写出发生中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O,
(2)小倩向上述剩余溶液中加入一定量的碳酸钠溶液,所得溶液中的溶质可能是什么?
猜想1:NaCl
猜想2:NaCl、HCl
猜想3:NaCl、HCl、CaCl2
猜想4:NaCl、CaCl2
猜想5:NaCl、Na2CO3(填化学式)
①经分析,小蒙认为猜想2不合理,理由是若有盐酸,则一定含有氯化钙,
②为验证其余猜想,小红做了以下实验:
| 实验内容 | 现象 | 结论 |
| 取样品少许于试管中,加入CaCO3粉末 | 有气泡产生 | 猜想3成立 |
7.甲、乙、丙、丁四种物质在一定条件下充分反应,测得反应前后各物质质量分数如图所示,下列说法正确的是( )


| A. | 丁一定是化合物 | |
| B. | 丙一定是这个反应的催化剂 | |
| C. | 该反应是分解反应 | |
| D. | 参加反应甲的质量等于生成的丙和乙的质量之和 |
17.下列实验操作中不正确的是( )
| A. |  熄灭酒精灯 | B. |  酸碱中和反应 | ||
| C. |  蒸发食盐水 | D. |  称量氢氧化钠固体 |

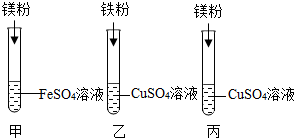 化学小组探究镁、铁、铜三种金属的活动性顺序,设计了下图所示实验方案.
化学小组探究镁、铁、铜三种金属的活动性顺序,设计了下图所示实验方案.