题目内容
两份等质量的碳酸钙,一份充分高温煅烧(CaCO3
CaO+CO2↑),另一份与足量盐酸反应,最终所得二氧化碳( )
| ||
| A、前者多后者少 | B、前者少后者多 |
| C、一样多 | D、无法判断 |
分析:根据反应的化学方程式,可得到两个反应中碳酸钙中的碳元素都全部转化为二氧化碳且二氧化碳中碳元素全部来自于碳酸钙,利用反应前后元素质量不变,可判断两个反应所产生二氧化碳的质量相等.
解答:解:碳酸钙高温锻烧的化学方程式为CaCO3
CaO+CO2↑;碳酸钙与盐酸反应的化学方程式为CaCO3+2HCl═CaCl2+CO2↑+H2O;
由反应的化学方程式可知,生成的二氧化碳中碳元素全部来自于碳酸钙,并且碳酸钙中的碳元素全部转化为二氧化碳;等质量的碳酸钙中碳元素的质量相等,因此,两个反应所生成二氧化碳气体的质量也相等;
故选C.
| ||
由反应的化学方程式可知,生成的二氧化碳中碳元素全部来自于碳酸钙,并且碳酸钙中的碳元素全部转化为二氧化碳;等质量的碳酸钙中碳元素的质量相等,因此,两个反应所生成二氧化碳气体的质量也相等;
故选C.
点评:对比两个反应,得出判断:生成的二氧化碳中碳元素全部来自于碳酸钙,并且碳酸钙中的碳元素全部转化为二氧化碳,这是解答本题的一种简便有效的方法.

练习册系列答案
相关题目
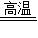 CaO+CO2↑),另一份与足量盐酸反应,最终所得二氧化碳( )
CaO+CO2↑),另一份与足量盐酸反应,最终所得二氧化碳( )