题目内容
16.实验室制取气体所需的装置如图所示.
请回答以下问题.
(1)实验仪器a的名称是铁架台;用高锰酸钾制取氧气时所选用的发生装置为B(填字母序号,下同);用大理石和稀盐酸制取二氧化碳所选用的收集装置为D.
(2)用过氧化氢溶液制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应的类型是分解反应.
(3)检查发生装置A气密性的方法是把导管口的下端浸入水中,用手紧握试管.如果观察到导管口有气泡冒出,则证明装置不漏气.
(4)已知F装置甲中吸有水,乙中吸有稀硫酸(H2SO4),烧杯①中盛有用石蕊溶液染成紫色的干燥纸花,烧杯②中盛有碳酸钠粉末.为了验证使石蕊变色的物质是碳酸而不是二氧化碳,应采取的实验操作是先向烧杯②中滴入稀硫酸,隔一定时间后再向烧杯①中滴入水,观察到的现象是开始干燥纸花不变色,滴入水后纸花变红色.
分析 (1)据常用仪器回答,加热高锰酸钾制取氧气属于固体加热型,故选发生装置B,二氧化碳密度比空气大且能溶于水,所以用向上排空气法收集;
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,据此书写方程式,该反应由一种物质生成两种物质,属于分解反应;
(3)据检查装置气密性的方法分析解答;
(4)根据稀硫酸与碳酸钠反应生成二氧化碳,二氧化碳与水接触形成碳酸、碳酸可使石蕊变红解答.
解答 解:(1)仪器a是固定仪器的铁架台;加热高锰酸钾制取氧气属于固体加热型,故选发生装置B,二氧化碳密度比空气大且能溶于水,所以用向上排空气法收集;
(2)过氧化氢在二氧化锰的催化作用下生成水和氧气,反应方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;该反应由一种物质生成两种物质,属于分解反应;
(3)检查A气密性可把导管口的下端浸入水中,用手紧握试管.如果观察到导管口有气泡冒出,则证明装置不漏气;
(4)要验证使石蕊变色的物质是碳酸而不是二氧化碳,可先向烧杯②中滴入稀硫酸,硫酸与碳酸钠反应产生二氧化碳,先让二氧化碳与干燥的纸花接触,隔一定时间观察花不变色,再向烧杯①中滴入水,让水与纸花接触,此时二氧化碳与水反应生成碳酸,纸花变红说明碳酸可使石蕊变色,而非二氧化碳;
故答案为:(1)铁架台; B;D;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.;分解反应;
(3)把导管口的下端浸入水中,用手紧握试管.如果观察到导管口有气泡冒出,则证明装置不漏气;
(4)先向烧杯②中滴入稀硫酸,隔一定时间后再向烧杯①中滴入水;开始干燥纸花不变色,滴入水后纸花变红色.
点评 本题难度不大,但综合性较强,掌握实验室制取气体的发生和收集装置选取方法、反应原理、反应类型判断、检查装置气密性的方法、二氧化碳的化学性质等是正确解答本题的关键.

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案| 选项 | 实验目的 | 实验设计 | |
| 实验一 | 实验二 | ||
| A | 探究铁、铜、银三种金属的活动性顺序 | 将铁丝放入2mL10%的硫酸铜溶液中 | 将银丝放入2mL10%的硫酸铜溶液中 |
| B | 催化剂对化学反应速率的影响 | 将带火星的木条伸入装有5mL5%过氧化氢溶液的试管中 | 将带火星的木条伸入装有少量红砖粉和5mL5%过氧化氢溶液的试管中 |
| C | 说明燃烧的条件之一 | 各取一小块同样大小的乒乓球和滤纸,分开放在一块薄铜片的两侧,加热铜片的中部 | 各取等体积的木屑绝碳粉,分开放在一块薄铁片的两侧,加热铁片的中部 |
| D | 人体吸入和呼出气体中二氧化碳含量的比较 | 向一瓶呼出的气体中伸入燃着的木条 | 向一瓶呼出的气体中倒入少量澄清石灰水 |
| A. | A | B. | B | C. | C | D. | D |
 如图所示,广口瓶内加入了一定量的固体,将胶头滴管中的液体滴加到广口瓶中的固体上,不能使b端液面明显卡簧的固体和液体组合是( )
如图所示,广口瓶内加入了一定量的固体,将胶头滴管中的液体滴加到广口瓶中的固体上,不能使b端液面明显卡簧的固体和液体组合是( )| A. | 锌粒和稀硫酸 | B. | 氢氧化钠固体和水 | ||
| C. | 生石灰固体和水 | D. | 硝酸铵固体和水 |
 ”表示氢原子,下列方框中能表示2H2的意义的是( )
”表示氢原子,下列方框中能表示2H2的意义的是( )| A. |  | B. | 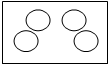 | C. | 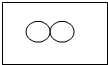 | D. | 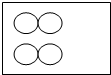 |
| A. | 滴加CaCl2溶液 | B. | 滴加稀盐酸 | C. | 滴加Ca(OH)2溶液 | D. | 滴加石蕊试液 |
| A. | 倒出仍是饱和食盐水 | B. | 倒出溶液的溶质质量分数变小了 | ||
| C. | 倒出溶液的溶解度变小 | D. | 倒出溶液的溶质质量分数变大了 |
 二氧化碳虽然只约占空气总体积的0.03%,但对动植物的生命活动起着极为重要的作用.自然界中二氧化碳的循环如右图所示,下列过程放在X处不合理的是( )
二氧化碳虽然只约占空气总体积的0.03%,但对动植物的生命活动起着极为重要的作用.自然界中二氧化碳的循环如右图所示,下列过程放在X处不合理的是( )| A. | 人和动物的呼吸 | B. | 发展利用氢燃料 | C. | 化石燃料的燃烧 | D. | 植物的呼吸作用 |
| A. | 燃放鞭炮 | B. | 禁止吸烟 | C. | 多开汽车 | D. | 乱扔垃圾 |
