题目内容
4.等质量的镁和锌分别放置在两只烧杯中,向两烧杯中分别加入质量分数相等的稀硫酸到过量,下图正确的是( )(相对原子质量:Mg-24,Zn-65)| A. | 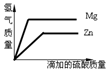 | B. | 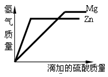 | C. | 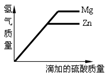 | D. | 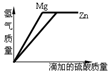 |
分析 题目给出的图是向等质量的金属中加入酸,由于酸的溶质质量分数相同,由于生成氢气的速度取决于滴加硫酸的速度,所以生成氢气的速度是相同的.由于产生的氢气的质量与其相对原子质量有关,等质量金属完全反应时,镁得到的氢气多,所以是镁消耗的酸多,对应的氢气也多.据此分析解答.
解答 解:题目给出的图是向等质量的金属中加入酸,由于酸的溶质质量分数相同,由于生成氢气的速度取决于滴加硫酸的速度,所以生成氢气的速度是相同的.而产生的氢气的质量与其相对原子质量有关:假设镁与锌的质量都为1克,根据化学方程式计算可知,则生成氢气的质量分别为$\frac{2}{24}$g、$\frac{2}{65}$g,显然镁与稀硫酸生成的氢气的质量较多.故最终生成的氢气镁大于锌,观察图象C符合题意;
故选:C.
点评 熟练掌握金属活动性顺序及其应用,学会处理有关题目;对于此类问题,可以设定特殊值:如假设镁与锌的质量都为1克,根据化学方程式计算进行计算,可知答案.

练习册系列答案
相关题目
14.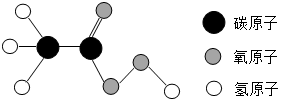 年我国部分地区突发了“非典型性肺炎”威胁着人们的身体健康.过氧乙酸可以起到消毒作用,其分子结构如图所示.下列有关过氧乙酸的下列叙述不正确的是( )
年我国部分地区突发了“非典型性肺炎”威胁着人们的身体健康.过氧乙酸可以起到消毒作用,其分子结构如图所示.下列有关过氧乙酸的下列叙述不正确的是( )
 年我国部分地区突发了“非典型性肺炎”威胁着人们的身体健康.过氧乙酸可以起到消毒作用,其分子结构如图所示.下列有关过氧乙酸的下列叙述不正确的是( )
年我国部分地区突发了“非典型性肺炎”威胁着人们的身体健康.过氧乙酸可以起到消毒作用,其分子结构如图所示.下列有关过氧乙酸的下列叙述不正确的是( )| A. | 过氧乙酸分子的化学式为 C2H4O3,其相对分子质量为 76 | |
| B. | 过氧乙酸是一种化合物 | |
| C. | C、H、O三种元素的质量比为 2:4:3 | |
| D. | 完全燃烧可能会生成 CO2 和 H2O |
15.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如表,对该反应,下列描述正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | m | 8 | 6 |
| 反应后质量/g | 4 | 待测 | 28 | 2 |
| A. | “待测”数值一定为2g | B. | 乙一定是该反应的催化剂 | ||
| C. | 反应中甲和丙的质量比为1:7 | D. | 该反应中甲、丁都是反应物 |
9.日前,美国两大玻璃制造商皮尔金顿和PPG分别宣布,他们利用纳米技术研制成功了新型的“自净玻璃”,解决了这个令千家万户挠头的问题.新型玻璃会自动“洗脸”、“美容”,保持明净.“自净玻璃”在自洁的同时,这种纳米涂层还能不断分解甲醛、苯、氨气等有害气体,杀灭室内空气中的各种细菌和病毒,有效地净化空气,减少污染.下列关于甲醛(HCHO)的叙述正确的是( )
| A. | 甲醛由四种元素组成 | |
| B. | 甲醛中氢元素和氧元素的质量比为2:1 | |
| C. | 甲醛属于有机化合物 | |
| D. | 甲醛分子由一个氢分子和一个一氧化碳分子构成 |
16.下列有关实验设计和操作的叙述中,不正确的是( )
| A. | 某化肥与碱共热,若产生使湿润红色石蕊试纸变蓝的气体,证明为铵盐氮肥 | |
| B. | 将Fe(OH)3加入到滴有酚酞试液的蒸馏水中,溶液显红色 | |
| C. | 实验室做氢气还原氧化铁的实验时,应先通入氢气,过一会儿再给氧化铁加热 | |
| D. | 配制溶液时必须使用的仪器有托盘天平、量筒、烧杯、玻璃棒等 |
14.20℃食盐的溶解度为36g,20℃时将20g食盐放入50g 水中充分溶解后,所得溶液的溶质的质量分数是( )
| A. | 28.6% | B. | 26.5% | C. | 40% | D. | 30% |




 将氢气通入盛有氧化铜的试管中,加热一段时间后,可观察到试管中有红色固体出现
将氢气通入盛有氧化铜的试管中,加热一段时间后,可观察到试管中有红色固体出现