题目内容
16.认真阅读下面资料,回答相关问题:1807年,科学家首次利用电解氢氧化钠的方法制备金属钠,同时得到氧气和水.1921年,科学家通过电解熔融氯化钠的方法制备金属钠同样获得成功.
金属钠很软,可以用小刀切割,切开外皮后,可以看到钠具有银白色的金属光泽,很快就会被氧化失去光泽.钠的密度是0.97g/cm3,比水的密度小,比煤油密度大,保存在盛有煤油的试剂瓶中.用镊子取一小块金属钠,用滤纸吸干表面的煤油,用小刀切去一端的表层,放入滴加过几滴酚酞试液的水中,可观察到钠浮在水面上,熔成闪亮的小球,在水面上来回游动,发出“嘶嘶”的响声,溶液会变红.收集反应后产生的气体,经检验发现其具有可燃性.
工业上用钠作还原剂,用于冶炼金属,如4Na+TiCl4$\frac{\underline{\;熔融\;}}{\;}$+4NaCl;Na-K合金(液态)用作原子反应堆的导热剂;在电光源上,用钠制造高压钠灯.
(1)制备金属钠的方法是电解氢氧化钠或电解熔融氯化钠.
(2)钠的物理性质有银白色、很软等(需答出2点).
(3)能说明钠遇水生成气体的现象是在水面上来回游动,发出“嘶嘶”的响声.
(4)钠与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
(5)实验室中的金属钠通常保存在煤油中的原因是BCD.(填字母序号)
A.钠是金属 B.常温下钠能与氧气反应
C.常温下钠能与水反应 D.钠比煤油的密度(0.8g/cm3)大.
分析 根据题目给出的信息分析解答本题.
解答 解;(1)根据题目所给信息可知,制备金属钠的方法有电解氢氧化钠或电解熔融氯化钠;
(2)物理性质是物质不需要经过化学变化就能表现出来的性质,钠很软,具有银白色的金属光泽,密度是0.97g/cm3等都是钠的物理性质;
(3)钠浮在水面上,熔成闪亮的小球,在水面上来回游动,发出“嘶嘶”的响声,说明钠与水反应生成气体;
(4)钠与水反应生成氢氧化钠和氢气,反应的化学方程式为:2Na+2H2O=2NaOH+H2↑;
(5)金属钠异常活泼,所以要保存到煤油中,原因是在常温下它即能与氧气反应、又能与水反应,它的密度大于煤油的密度,所以常保存在煤油中.
故答案为:(1)电解氢氧化钠或电解熔融氯化钠;
(2)银白色、很软(密度0.97g/cm3);
(3)在水面上来回游动,发出“嘶嘶”的响声;
(4)2Na+2H2O=2NaOH+H2↑;
(5)BCD;
点评 本题属于信息分析题,题目难度不大,细致分析即可正确解答.

练习册系列答案
相关题目
6.如图表示初中化学常见物质的相互转化关系(反应条件已省略).下列说法错误的是( )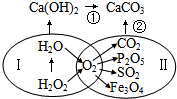

| A. | 圈I中发生的反应可能都是分解反应 | |
| B. | 利用反应②可用来检验二氧化碳气体 | |
| C. | 圈Ⅱ中的化学反应说明氧气具有可燃性 | |
| D. | 利用反应①可制得烧碱 |
4.化学实验操作直接影响实验结果和人身安全,下列关于实验操作的说法正确的是( )
| A. | 用100mL的量筒量取8.5mL的水 | |
| B. | 称量固体药品时,左盘放砝码,右盘放物体 | |
| C. | 稀释浓硫酸时,将水沿烧杯内壁注入盛有浓硫酸的烧杯中,并用玻璃棒不断搅拌 | |
| D. | 点燃可燃性气体前必须检验纯度 |
11.下列物品所使用的主要材料属于金属材料的是( )
| A. |  橡胶轮胎 | B. |  木雕作品 | C. |  艺术瓷瓶 | D. |  青铜摆件 |
3.为除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | HCl(CO2) | 适量NaOH溶液 | 洗气 |
| B | NaCl(NaOH) | 过量稀盐酸 | 蒸发结晶 |
| C | CO2(CO) | 足量O2 | 点燃 |
| D | CaO固体(CaCO3) | 足量的水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
20.如图所示实验有关说法或得出的结论不合理的是( )
| A. |  可探究可燃物燃烧的两个条件 | |
| B. |  可以说明微粒是不停运动的,还能说明氨气具有碱性 | |
| C. |  铁丝也会生锈,生锈后U型管中液面左高右低 | |
| D. |  既可以说明一氧化碳能与氧化铁反应,又可以说明一氧化碳具有可燃性 |