题目内容
12. 某化工厂用侯氏制碱法制得的纯碱中含少量氯化钠.为了测定纯碱样品中碳酸钠的质量,化学兴趣小组的同学进行了以下实验:
某化工厂用侯氏制碱法制得的纯碱中含少量氯化钠.为了测定纯碱样品中碳酸钠的质量,化学兴趣小组的同学进行了以下实验:①取该纯碱样品12.7g,加入150g水中,充分搅拌到完全溶解;
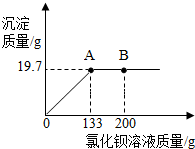
②向①中所得溶液里逐滴滴加某未知溶质质量分数的氯化钡溶液,通过观察现象,记录数据后绘制的图表如图所示,横坐标表示加入的氯化钡溶
液质量,纵坐标表示生成沉淀的质量.请根据以上所述,
回答下列问题:
(1)当滴入氯化钡溶液至图中B点时,烧杯中溶液里含有的溶质是(写化学式)BaCl2、NaCl
(2)所加氯化钡溶液中溶质的质量分数是多少?(计算结果精确至0.1%).
分析 根据碳酸钠和氯化钡会生成碳酸钡沉淀,结合图象中的转折点进行分析;
根据方程式中的比例关系和题中的数据解出需要的数据.
解答 解:(1)当氯化钡和碳酸钠接触后会生成碳酸钙沉淀和氯化钠,加入的氯化钡质量大于133克时,沉淀质量不再变化,所以A点两者恰好完全反应,B点时,氯化钡过量,含有的溶质有样品中的氯化钠、生成的氯化钠,和过量的氯化钡;
(2)从图象中可以看出加入133克的氯化钡时生成的沉淀质量是19.7克,
设参加反应的氯化钡质量为x,
Na2CO3+BaCl2=2NaCl+BaCO3↓
106 208 117 197
x 19.7g
$\frac{208}{x}$=$\frac{197}{19.7g}$
x=20.8g
所以所加氯化钡溶液中溶质的质量分数是:$\frac{20.8g}{133g}$×100%=15.6%.
故答案为:(1)BaCl2、NaCl;
(2)15.6%.
点评 在解此类题时,关键是分析题中图象中转折点的含义和方式反应的原理,再根据比例关系解答.

练习册系列答案
相关题目
9.下列实验的基本操作正确的是( )
| A. | 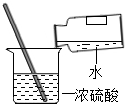 浓硫酸的稀释 | B. | 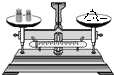 称量一定质量的食盐 | ||
| C. | 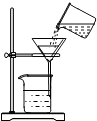 过滤 | D. | 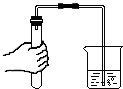 检查装置的气密性 |
3.人们在认识事物时可以采取多种方法,多种角度,下面对硝酸认识不正确的是( )
| A. | 硝酸铵是一种氮肥 | B. | 硝酸铵是一种氧化物 | ||
| C. | 硝酸铵中氮元素的化合价不同 | D. | 硝酸铵属于盐类 |
7.化学学科的思维方法有多种,其中推理是最常见的一种思维方法.以下推理正确的是( )
| A. | 酸溶液中一定含有氢离子,含有氢离子的溶液一定是酸溶液 | |
| B. | 有机物一定含有碳元素,含有碳元素的化合物不一定是有机化合物 | |
| C. | 氧化物由氧元素和另一种元素组成,则仅含氧元素及另一种元素的物质一定是氧化物 | |
| D. | 铁和银均为金属,铁与稀盐酸反应生成氢气,则银也能与稀盐酸反应生成氢气 |
1.运输浓硫酸时,应在贮罐上贴的标识是( )
| A. |  | B. |  | C. |  | D. |  |
2.测定人体内体液的pH可以帮助我们了解身体状况.如图是明明同学体检报告单截图,看图后回答问题.
(1)该同学哪项指标出现异常胃液pH偏小.
(2)医生让明明服用一种主要成分为氢氧化铝的药物,请写出该反应的化学方程式Al(OH)3+3HCl=AlCl3+3H2O.
(3)明明服用的药物,可用厨房中的一种物质代替,这种物质是小苏打(或碳酸氢钠).
| 项目 | 检测值 | 正常pH范围 |
| 血浆 | 7.41 | 7.35~7.45 |
| 胃液 | 0.8↓ | 0.9~1.5 |
| 胆汁 | 7.21 | 7.1~7.3 |
| 胰液 | 7.8 | 7.5~8.0 |
(2)医生让明明服用一种主要成分为氢氧化铝的药物,请写出该反应的化学方程式Al(OH)3+3HCl=AlCl3+3H2O.
(3)明明服用的药物,可用厨房中的一种物质代替,这种物质是小苏打(或碳酸氢钠).